题目内容
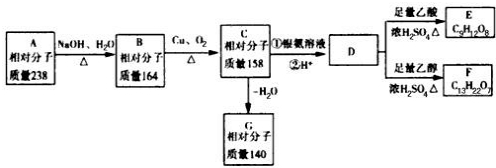 A、B、C、D、E、F、G都是链状有机物,它们的转化关系如图所示,A只含一种官能团,D的相对分子质量与E相差42,D的核磁共振氢谱图上有3个峰,且峰面积之比为1:3:6,请回答下列问题;
A、B、C、D、E、F、G都是链状有机物,它们的转化关系如图所示,A只含一种官能团,D的相对分子质量与E相差42,D的核磁共振氢谱图上有3个峰,且峰面积之比为1:3:6,请回答下列问题;(1)A中含有的官能团是
(2)写出D的结构简式
(3)写出B生成C的化学方程式
(4)C生成G的反应类型
(5)芳香族化合物H与G互为同分异构体,1mol H与足量氢氧化钠溶液反应消耗2mol NaOH,1molH最多消耗3molNa,且H苯环上的一氯代物只有两种,写出两种符合条件的H的结构简式:
考点:有机物的推断
专题:有机物的化学性质及推断
分析:由转化关系可知,A在NaOH水溶液、加热条件下生成B,B在Cu、氧气加热条件下生成C,故B为醇,则C含有-CHO或羰基,C氧化生成D,D能与乙酸、乙醇反应,故D含有羧基-COOH、羟基-OH,故B中含有不能被氧化的-OH,由B、C的相对分子质量可知,B中能被氧化的-OH数目为(164-158)÷2=3,故B中至少含有4个-OH.由E、F中C原子数目可知,D中-COOH比-OH多2个,由F中氧原子可知D中最多有3个-COOH,故D中含有3个-COOH、1个-OH,故D中含有7个碳原子,C中含有3个-CHO、1个-OH,由转化关系可知B、C、D中碳原子数目相等,都为7个,故C中剩余基团的式量为158-17-29×3-12×(7-3)=6,故C中还含有6个H原子,C的分子式为C7H10O4,C氧化为D,-CHO转化为-COOH,故D为C7H10O7,D分子中不含甲基,D的核磁共振氢谱图上有3个峰,且峰面积之比为1:3:6,故D的结构简式为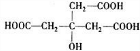 ,逆推可得C的结构简式为
,逆推可得C的结构简式为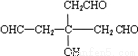 、B为
、B为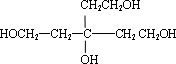 ,故G为
,故G为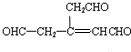 ,E为
,E为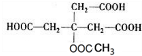 ,F为
,F为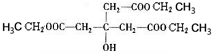 .A为含有四个相同卤原子的卤代烃且分子中无甲基,A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为
.A为含有四个相同卤原子的卤代烃且分子中无甲基,A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为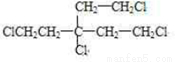 ,据此解答.
,据此解答.
 ,逆推可得C的结构简式为
,逆推可得C的结构简式为 、B为
、B为 ,故G为
,故G为 ,E为
,E为 ,F为
,F为 .A为含有四个相同卤原子的卤代烃且分子中无甲基,A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为
.A为含有四个相同卤原子的卤代烃且分子中无甲基,A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为 ,据此解答.
,据此解答.解答:
解:由转化关系可知,A在NaOH水溶液、加热条件下生成B,B在Cu、氧气加热条件下生成C,故B为醇,则C含有-CHO或羰基,C氧化生成D,D能与乙酸、乙醇反应,故D含有羧基-COOH、羟基-OH,故B中含有不能被氧化的-OH,由B、C的相对分子质量可知,B中能被氧化的-OH数目为(164-158)÷2=3,故B中至少含有4个-OH.由E、F中C原子数目可知,D中-COOH比-OH多2个,由F中氧原子可知D中最多有3个-COOH,故D中含有3个-COOH、1个-OH,故D中含有7个碳原子,C中含有3个-CHO、1个-OH,由转化关系可知B、C、D中碳原子数目相等,都为7个,故C中剩余基团的式量为158-17-29×3-12×(7-3)=6,故C中还含有6个H原子,C的分子式为C7H10O4,C氧化为D,-CHO转化为-COOH,故D为C7H10O7,D分子中不含甲基,D的核磁共振氢谱图上有3个峰,且峰面积之比为1:3:6,故D的结构简式为 ,逆推可得C的结构简式为
,逆推可得C的结构简式为 、B为
、B为 ,故G为
,故G为 ,E为
,E为 ,F为
,F为 .A为含有四个相同卤原子的卤代烃且分子中无甲基,A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为
.A为含有四个相同卤原子的卤代烃且分子中无甲基,A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为 ,
,
(1)A为 ,含有的官能团为氯原子,故答案为:氯原子;
,含有的官能团为氯原子,故答案为:氯原子;
(2)由上述分析可知,D的结构简式为 ,故答案为:
,故答案为: ;
;
(3)B生成C的化学方程式为: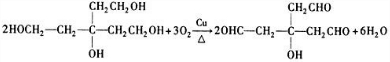 ,
,
故答案为: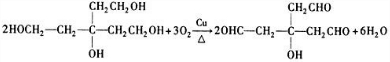 ;
;
(4)C( )生成G(
)生成G( )的反应类型为消去反应,C生成G有1种产物,故答案为:消去反应;1;
)的反应类型为消去反应,C生成G有1种产物,故答案为:消去反应;1;
(5)芳香族化合物H与G( )互为同分异构体,G的不饱和度为4,故H含有1个苯环,侧链不存在不饱和键,1molH与足量氢氧化钠溶液反应消耗2molNaOH,且1molH最多消耗3molNa,则H分子含有2故酚羟基、1个醇羟基,若H苯环上的一氯代物只有两种,所有符合条件的H的结构简式为:
)互为同分异构体,G的不饱和度为4,故H含有1个苯环,侧链不存在不饱和键,1molH与足量氢氧化钠溶液反应消耗2molNaOH,且1molH最多消耗3molNa,则H分子含有2故酚羟基、1个醇羟基,若H苯环上的一氯代物只有两种,所有符合条件的H的结构简式为:
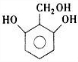 、
、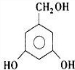 ,故答案为:
,故答案为: 、
、 .
.
 ,逆推可得C的结构简式为
,逆推可得C的结构简式为 、B为
、B为 ,故G为
,故G为 ,E为
,E为 ,F为
,F为 .A为含有四个相同卤原子的卤代烃且分子中无甲基,A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为
.A为含有四个相同卤原子的卤代烃且分子中无甲基,A分子中只含有一种官能团,水解引入-OH得到B,将-OH还原为A中的基团(或原子),令A中代替-OH的基团(或原子)式量为a,则4a+(164-4×17)=238,解得a=35.5,故为Cl原子,则A为 ,
,(1)A为
 ,含有的官能团为氯原子,故答案为:氯原子;
,含有的官能团为氯原子,故答案为:氯原子;(2)由上述分析可知,D的结构简式为
 ,故答案为:
,故答案为: ;
;(3)B生成C的化学方程式为:
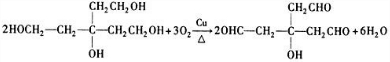 ,
,故答案为:
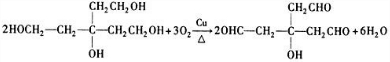 ;
;(4)C(
 )生成G(
)生成G( )的反应类型为消去反应,C生成G有1种产物,故答案为:消去反应;1;
)的反应类型为消去反应,C生成G有1种产物,故答案为:消去反应;1;(5)芳香族化合物H与G(
 )互为同分异构体,G的不饱和度为4,故H含有1个苯环,侧链不存在不饱和键,1molH与足量氢氧化钠溶液反应消耗2molNaOH,且1molH最多消耗3molNa,则H分子含有2故酚羟基、1个醇羟基,若H苯环上的一氯代物只有两种,所有符合条件的H的结构简式为:
)互为同分异构体,G的不饱和度为4,故H含有1个苯环,侧链不存在不饱和键,1molH与足量氢氧化钠溶液反应消耗2molNaOH,且1molH最多消耗3molNa,则H分子含有2故酚羟基、1个醇羟基,若H苯环上的一氯代物只有两种,所有符合条件的H的结构简式为: 、
、 ,故答案为:
,故答案为: 、
、 .
.
点评:本题考查有机物推断,需要学生充分利用分子式、相对原子质量综合分析各物质含有的官能团、C原子数目等进行推断,是对学生综合能力的考查,难度较大.

练习册系列答案
相关题目
除去下列各物质中混有的少量杂质,所用试剂不正确的是( )
| 序号 | 物 质 | 杂 质 | 所 用 试 剂 |
| A | N2 | O2 | 灼热的铜网 |
| B | CO2 | H2O | 浓硫酸 |
| C | CaO | CaCO3 | 适量的稀盐酸 |
| D | NaCl溶液 | Na2CO3 | 适量的稀盐酸 |
| A、A | B、B | C、C | D、D |
下列各种变化中,不能通过一步反应就能实现的是( )
| A、Al2O3→Al(OH)3 |
| B、FeCl3→FeCl2 |
| C、Fe(OH)2→Fe(OH)3 |
| D、Al→AlO2- |
700℃时,H2(g)+CO2(g)?H2O(g)+CO(g).该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示.其中甲经2min达平衡时,v(H2O)为0.025mol/(L?min),下列判断不正确的是( )
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.10 | 0.20 | 0.20 |
| c(CO2)/mol/L | 0.10 | 0.10 | 0.20 |
| A、平衡时,乙中CO2的转化率大于50% | ||
| B、当反应平衡时,丙中c(CO2)是甲中的2倍 | ||
C、温度升至800℃,上述反应平衡常数为
| ||
| D、其他条件不变,若起始时向容器乙中充入0.10mol/L H2和0.20 mol/L CO2,到达平衡时c (CO)与乙不同 |