题目内容
黄铜矿主要成分是二硫化亚铁铜(CuFeS2).黄铜矿经熔炼、煅烧后得到粗铜和炉渣,冶炼过程的主要反应有:
①2CuFeS2+O2
Cu2S+2FeS+SO2
②Cu2S+O2
2Cu+SO2
(1)二硫化亚铁铜也可以表示为CuS?FeS,其中硫元素的化合价是 .
(2)反应②中还原剂是 .
(3)某校学习小组用炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3等)制备铁红,进行如下实验.
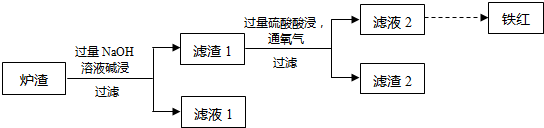
①炉渣碱浸时反应的离子方程式是 、 .
②滤渣1中加入硫酸并通入氧气可使FeO转化为Fe3+,该反应的离子方程式是 ;为检验铁元素是否被氧化完全,应进行的实验是:取少量滤液2于试管中, .
①2CuFeS2+O2
| ||
②Cu2S+O2
| ||
(1)二硫化亚铁铜也可以表示为CuS?FeS,其中硫元素的化合价是
(2)反应②中还原剂是
(3)某校学习小组用炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3等)制备铁红,进行如下实验.

①炉渣碱浸时反应的离子方程式是
②滤渣1中加入硫酸并通入氧气可使FeO转化为Fe3+,该反应的离子方程式是
考点:铜金属及其重要化合物的主要性质,物质分离和提纯的方法和基本操作综合应用
专题:元素及其化合物
分析:(1)二硫化亚铜也可以表示为CuS-FeS,其中硫元素的化合价为-2价;
(2)反应②中Cu2S中铜元素的化合价由+1价升高到+2价,作还原剂;
(3)①根据题目的流程图可知,炉渣中加入过量的氢氧化钠,二氧化硅、氧化铝都会溶解;
②炉渣1中加入硫酸并通入氧气可使FeO转化为Fe3+;为检验铁元素是否被氧化完全,可检验滤液中是否含有Fe2+.
(2)反应②中Cu2S中铜元素的化合价由+1价升高到+2价,作还原剂;
(3)①根据题目的流程图可知,炉渣中加入过量的氢氧化钠,二氧化硅、氧化铝都会溶解;
②炉渣1中加入硫酸并通入氧气可使FeO转化为Fe3+;为检验铁元素是否被氧化完全,可检验滤液中是否含有Fe2+.
解答:
解:(1)二硫化亚铜也可以表示为CuS-FeS,其中硫元素的化合价为-2价,故答案为:-2;
(2)反应②中Cu2S中铜元素的化合价由+1价升高到+2价,作还原剂;故答案为:Cu2S;
(3)①根据题目的流程图可知,炉渣中加入过量的氢氧化钠,二氧化硅、氧化铝都会溶解;故答案为:SiO2+2OH-=SiO32-+H2O;Al2O3+2OH-=2AlO2-+H2O;
②炉渣1中加入硫酸并通入氧气可使FeO转化为Fe3+;为检验铁元素是否被氧化完全,可检验滤液中是否含有Fe2+;应进行的实验是:滴入2~3滴K3[Fe(CN)6]溶液,若有蓝色沉淀产生,则氧化不完全,反之则氧化完全;
故答案为:4FeO+O2+12H+=4Fe3++6H2O;滴入2~3滴K3[Fe(CN)6]溶液,若有蓝色沉淀产生,则氧化不完全,反之则氧化完全.
(2)反应②中Cu2S中铜元素的化合价由+1价升高到+2价,作还原剂;故答案为:Cu2S;
(3)①根据题目的流程图可知,炉渣中加入过量的氢氧化钠,二氧化硅、氧化铝都会溶解;故答案为:SiO2+2OH-=SiO32-+H2O;Al2O3+2OH-=2AlO2-+H2O;
②炉渣1中加入硫酸并通入氧气可使FeO转化为Fe3+;为检验铁元素是否被氧化完全,可检验滤液中是否含有Fe2+;应进行的实验是:滴入2~3滴K3[Fe(CN)6]溶液,若有蓝色沉淀产生,则氧化不完全,反之则氧化完全;
故答案为:4FeO+O2+12H+=4Fe3++6H2O;滴入2~3滴K3[Fe(CN)6]溶液,若有蓝色沉淀产生,则氧化不完全,反之则氧化完全.
点评:本题考查了物质制备过程分析判断,物质性质的理解应用,化学方程式和离子方程式书写方法,掌握基础是关键,题目难度中等.

练习册系列答案
 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1,测得0到10秒内,c(H2)减小了0.75mol?L-1,下列说法正确的是( )
| A、10到15秒内c(NH3) 增加量等于0.25mol?L-1 |
| B、10秒内氨气的平均反应速率为0.025mol?L-1?s-1 |
| C、达平衡后,分离出少量NH3,v正增大 |
| D、该反应的逆反应的活化能不小于92.2kJ?mol-1 |
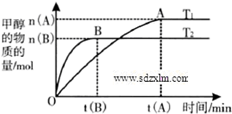 到2013午云南已连续4年干旱,专家认为云南和其他城市一样受到全球变暖的气候变化影响.CO2等温室气体是导致全球变暖的主要原因,控制和治理CO2是解决温室效应的有效途径.
到2013午云南已连续4年干旱,专家认为云南和其他城市一样受到全球变暖的气候变化影响.CO2等温室气体是导致全球变暖的主要原因,控制和治理CO2是解决温室效应的有效途径.
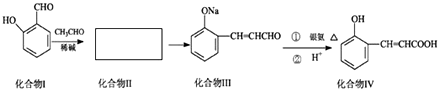
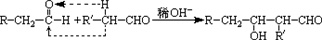
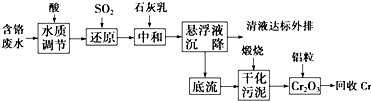 含铬废水、铬渣对环境的污染问题备受关注,通过化学原理对废物进行有效处理变废为宝是目前的一个重要研究课题.
含铬废水、铬渣对环境的污染问题备受关注,通过化学原理对废物进行有效处理变废为宝是目前的一个重要研究课题.