��Ŀ����
2����ѧʵ����е�ⱥ��ʳ��ˮʱ�ɴ�ͼ��ѡ�ñ�Ҫ��װ�ã���Ҫ��ⶨ�������������������25mL�����ͼ��������������ԣ�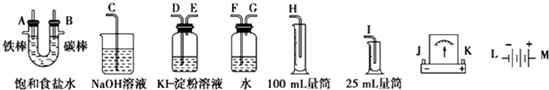
��1��д����ⱥ��ʳ��ˮ�����ӷ���ʽ2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2����
�� 2 ����Դ����������A������������ȷ����˳��Ϊ��L��A��B��J��K��M��
��3����ʵ��ⶨ�������������ʱ��ѡ�õ���ͲΪ50mL��Ͳ����25mL��Ͳ��50mL��Ͳ��
���� ��1��Ҫ��������̼����������Ȼ�����Һ��ȡ������������������̼���������������������ӷŵ����������������������ӷŵ�����������
��2����Դ�����ӵ��ص�������̼���ӵ����ơ�-���ˣ���+���˽ӵ�Դ������
��3�������������������25mL��
��� �⣺��1��Ҫ��������̼����������Ȼ�����Һ��ȡ������������������̼�����������������������ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ2H++2e-�TH2��������̼����������ʧ���ӷ���������Ӧ���缫��ӦʽΪ2Cl--2e-�TCl2����ͬʱ��Һ�л������������ƣ����Ե�ط�ӦʽΪ 2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$2NaOH+H2��+Cl2�������ӷ���ʽΪ2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2����
�ʴ�Ϊ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2����
��2����Դ�����ӵ��ص�������̼���ӵ����ơ�-���ˣ���+���˽ӵ�Դ����������������˳����A��B��J��K��
�ʴ�Ϊ��A��B��J��K��
��3�������������������25mL��Ӧѡ��50mL����Ͳ���ʴ�Ϊ��50mL��Ͳ��
���� �����Ե��ԭ��Ϊ���忼�����������ȡ�����ʵļ����֪ʶ�㣬���ݵ��ԭ�������ʵ����ʵ���������ɣ��ѵ�����������˳���Ѷ��еȣ�

| A�� | 44.8 L����������ֽ��22.4 L��������22.4 L�ķ�������546.6 kJ���� | |
| B�� | 1 mol������1 mol������Ӧ����2 molҺ̬������ų�����������546.6 kJ | |
| C�� | ��ͬ�����£�1 mol������1 mol�����������ܺ���2 mol��������������� | |
| D�� | 2 mol H-F���ļ��ܱ�1 mol H-H����1 mol F-F ���ļ���֮�ʹ�546.6 kJ |
| A�� | Al3+��CH3COO-��Cl- | B�� | Mg2+��Ba2+��Br- | ||
| C�� | Mg2+��Cl-��I- | D�� | Na+��NH4+��Cl- |
| A�� | $\frac{b}{2a}$mol-1 | B�� | $\frac{a}{4b}$mol-1 | C�� | $\frac{a}{b}$mol-1 | D�� | $\frac{b}{a}$mol-1 |
| A�� | Zn��s��+CuSO4��aq��=ZnSO4��aq��+Cu��s����H=-216 kJ•mol-1����Ӧ���������������������� | |
| B�� | ��ͬ�����£����1 mol��ԭ�������е�����ΪE1��1 mol ����������е�����ΪE2����2E1=E2 | |
| C�� | 101 kPaʱ��2H2��g��+O2��g��=2H2O��l����H=-571.6 kJ•mol-1����H2��ȼ����Ϊ571.6 kJ•mol-1 | |
| D�� | H+��aq��+OH-��aq��=H2O��l����H=-57.3 kJ•mol-1����1 mol NaOH���������ƹ����뺬0.5 mol H2SO4��ϡ�����Ϻ�ų�57.3 kJ������ |
| A�� | ��Ӧ�������������� | |
| B�� | NH4CuSO3����Ԫ�ر����� | |
| C�� | �̼�����ζ�������ǰ��� | |
| D�� | 1mol NH4CuSO3��ȫ��Ӧת��0.5mol���� |
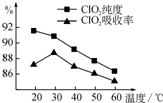 ij�о�С���û�����FeS2���������ƺ�������Һ��Ϸ�Ӧ�Ʊ�ClO2���壬����ˮ���ո�����ɵ�ClO2��Һ���ڴ˹�������Ҫ�������˵��¶ȣ����¶Ȳ���������Ӧ���ӣ�Ӱ������ClO2����Ĵ��ȣ��һ�Ӱ��ClO2�������ʣ����������ͼ��ʾ��
ij�о�С���û�����FeS2���������ƺ�������Һ��Ϸ�Ӧ�Ʊ�ClO2���壬����ˮ���ո�����ɵ�ClO2��Һ���ڴ˹�������Ҫ�������˵��¶ȣ����¶Ȳ���������Ӧ���ӣ�Ӱ������ClO2����Ĵ��ȣ��һ�Ӱ��ClO2�������ʣ����������ͼ��ʾ��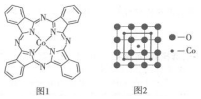 ������ѧ�����ʽṹ�����֪ʶ�ش��������⣺
������ѧ�����ʽṹ�����֪ʶ�ش��������⣺