题目内容
9.与“实验操作”相对应的“实验现象”的字母代号填入答案栏中| 实验操作 | 答案 | 实验现象 |
| (1)将浓硫酸滴在小木条上 | A.产生白烟 | |
| (2)将分别蘸有浓氨水和浓盐酸的玻璃棒靠近 | B.溶液褪色 | |
| (3)在盛有KI淀粉溶液的试管中滴加氯水 | C.溶液呈红色 | |
| (4)在盛有FeCl3溶液的试管中滴入2滴KSCN溶液 | D.产生棕红色气体 | |
| (5)铜丝放到浓硝酸中 | E.变黑色 | |
| (6)铜丝放入热的浓硫酸溶液中,将生成气体通入品红溶液中 | F.产生蓝色物质 |
分析 (1)浓硫酸具有强氧化性,能将纤维素中的H、O元素以2:1水的形式脱去而体现脱水性;
(2)浓氨水和浓盐酸都具有挥发性,二者相遇立即反应生成氯化铵固体而产生白烟;
(3)氯气具有强氧化性,能氧化碘离子生成碘,碘遇淀粉试液变蓝色;
(4)氯化铁和KSCN发生络合反应生成络合物硫氰化铁而导致溶液呈血红色;
(5)铜与浓硝酸反应生成红棕色的二氧化氮气体;
(6)铜与浓硫酸反应生成二氧化硫气体,二氧化硫具有漂白性,能够使品红溶液褪色.
解答 解:(1)浓硫酸具有强氧化性,能将纤维素中的H、O元素以2:1水的形式脱去而体现脱水性,最后将纤维素氧化为黑色的碳,则E正确,
故答案为:E;
(2)浓氨水和浓盐酸都具有挥发性,二者相遇立即反应生成氯化铵固体而产生白烟,所以看到的现象是产生白烟,则A正确,
故答案为:A;
(3)氯气具有强氧化性,能氧化碘离子生成碘,碘遇淀粉试液变蓝色,所以看到的现象是产生蓝色物质,则F正确,
故答案为:F;
(4)氯化铁和KSCN发生络合反应生成络合物硫氰化铁而导致溶液呈血红色,所以看到的现象是:溶液由黄色转化为血红色,则C正确,
故答案为:C;
(5)铜丝放到浓硝酸中,二者反应生成硝酸铜、二氧化氮气体和水,则反应中有红棕色气体生成,则D正确,
故答案为:D;
(6)铜丝放入热的浓硫酸溶液中生成二氧化硫,二氧化硫具有漂白性,将二氧化硫通入品红溶液中,品红溶液褪色,则B正确,
故答案为:B.
点评 本题考查了常见元素及其化合物性质,为高频考点,题目难度中等,明确常见物质性质是解本题关键,注意掌握铁离子、碘离子检验方法及现象,试题培养了学生的化学实验能力.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
19.反应3H2+N2$?_{催化剂}^{高温,高压}$2NH3在密闭容器中进行.下列关于该反应的说法错误的是( )
| A. | 升高温度能加快反应速率 | |
| B. | 使用恰当的催化剂能加快反应速率 | |
| C. | 增大N2的浓度能加快反应速率 | |
| D. | 平衡时各组分含量之比一定等于3:1:2 |
20.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,2.24 L CO2与一定量的Na2O2反应转移的电子数目一定为0.1NA | |
| B. | C2H2、H2O2、Na2O2的最简式都可以用AB的形式表示 | |
| C. | 50 mL 12 mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| D. | 2.0 gH218O与D216O的混合物中所含中子数为NA |
17.下列关于定量实验中的基本操作和仪器的描述正确的是( )
| A. | 用托盘天平称取20.00 g NaOH固体 | |
| B. | 向用水润湿的pH试纸上滴盐酸,可测定盐酸的pH | |
| C. | 用电子分析天平测得铁片质量是15.524 g | |
| D. | 在配制一定物质的量浓度的溶液时,定容后,经摇匀发现液面低于刻度线,此时再加入蒸馏水使其液面与刻度线持平 |
14.目前使用最多的气体石化燃料是( )
| A. | 煤 | B. | 石油 | C. | 天然气 | D. | CO |
1.某兴趣小组的同学发现,将CuSO4溶液与K2CO3溶液混合会产生蓝绿色沉淀.他们对沉淀的组成很感兴趣,决定采用实验的方法进行探究.
(1)【提出假设】假设1:所得沉淀为Cu(OH)2;
假设2:所得沉淀为CuCO3;(填化学式)
假设3:所得沉淀为碱式碳酸铜[化学式可表示为mCu(OH)2•nCuCO3].
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水).
【定性探究】
步骤1:将所得悬浊液过滤,先用蒸馏水洗涤,再用无水乙醇洗涤,风干;
步骤2:甲同学取一定量固体,用气密性良好的如装置如图(夹持仪器未画)进行定性实验;
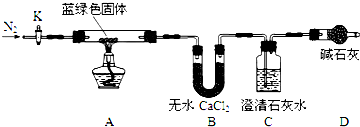
(2)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设1成立.
(3)乙同学认为只要将上图中B装置的试剂改用下列某试剂后,便可验证上述所有假设,该试剂是B(填代号).
A.浓硫酸 B.无水CuSO4 C.碱石灰 D.P2O5
(4)乙同学验证假设3成立的实验现象是A中蓝绿色固体变黑色,B中无水CuSO4固体变蓝,C中有白色沉淀产生.
【定量探究】
(5)乙同学进一步探究假设3中固体的组成:
①乙同学查得一些物质在常温时的数据(如下表)后,将C中的澄清石灰水改为Ba(OH)2溶液,其原因是AC(填代号).
A.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收CO2
B.Ba(OH)2为强碱,Ca(OH)2为弱碱
C.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
D.相同条件下,CaCO3的溶解度明显大于BaCO3
②若所取蓝绿色固体质量为27.1g,实验结束后,装置B的质量增加2.7g,C中产生沉淀的质量为19.7g.则该蓝绿色固体的化学式为2CuCO3•3Cu(OH)2、或3Cu(OH)2•2CuCO3或Cu5(OH)6(CO3)2;A中发生反应的化学方程式为2CuCO3•3Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+3H2O↑+2CO2↑.
(1)【提出假设】假设1:所得沉淀为Cu(OH)2;
假设2:所得沉淀为CuCO3;(填化学式)
假设3:所得沉淀为碱式碳酸铜[化学式可表示为mCu(OH)2•nCuCO3].
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水).
【定性探究】
步骤1:将所得悬浊液过滤,先用蒸馏水洗涤,再用无水乙醇洗涤,风干;
步骤2:甲同学取一定量固体,用气密性良好的如装置如图(夹持仪器未画)进行定性实验;

(2)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设1成立.
(3)乙同学认为只要将上图中B装置的试剂改用下列某试剂后,便可验证上述所有假设,该试剂是B(填代号).
A.浓硫酸 B.无水CuSO4 C.碱石灰 D.P2O5
(4)乙同学验证假设3成立的实验现象是A中蓝绿色固体变黑色,B中无水CuSO4固体变蓝,C中有白色沉淀产生.
【定量探究】
(5)乙同学进一步探究假设3中固体的组成:
①乙同学查得一些物质在常温时的数据(如下表)后,将C中的澄清石灰水改为Ba(OH)2溶液,其原因是AC(填代号).
| 溶解度(S)/p | 溶度积(Ksp) | 摩尔质量(M)/g•mol-1 | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
B.Ba(OH)2为强碱,Ca(OH)2为弱碱
C.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
D.相同条件下,CaCO3的溶解度明显大于BaCO3
②若所取蓝绿色固体质量为27.1g,实验结束后,装置B的质量增加2.7g,C中产生沉淀的质量为19.7g.则该蓝绿色固体的化学式为2CuCO3•3Cu(OH)2、或3Cu(OH)2•2CuCO3或Cu5(OH)6(CO3)2;A中发生反应的化学方程式为2CuCO3•3Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+3H2O↑+2CO2↑.
18.下列说法或表示方法中正确的是( )
| A. | 氢气的燃烧热为285.8kJ•mol-1,则氢气燃烧的热化学方程式为2H2(g)+02(g)=2H20(1)△H=-285kJ•mol-1 | |
| B. | 等质量的硫蒸气和硫粉分别完全燃烧,后者放出的热量多 | |
| C. | 某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应转移电子的数小于0.6×6.02×1023 | |
| D. | 已知中和热为57.3kJ•mol-1,若将含0.5molH2S04的浓硫酸溶液与含1mol Na0H的溶液混合,放出的热量要小于57.3kJ |
9.某学生用已知物质的量浓度的盐酸来测定未知浓度的氢氧化钠溶液时,选择甲基橙作指示剂,下列操作中可能使所测氢氧化钠溶液浓度偏大的是( )
| A. | 酸式滴定管未用标准盐酸润洗,直接装入标准盐酸 | |
| B. | 酸式滴定管滴定前有气泡,滴定后气泡消失 | |
| C. | 滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥 | |
| D. | 读取醋酸体积时,开始仰视读数,滴定结束后俯视读数 |
 或
或 .
.