题目内容
4.35g二氧化锰在100mL足量浓盐酸(密度为1.19g/cm3、质量分数为36.5%)中完全反应:MnO2+4HCl MnCl2+Cl2↑+2H2O。(Mn-55 O-16 H-1 Cl-35.5)
MnCl2+Cl2↑+2H2O。(Mn-55 O-16 H-1 Cl-35.5)
(1)表示上述氧化还原反应电子转移的方向和数目:__________________。
(2)浓盐酸中HCl的物质的量浓度:c(HCl)=___________。
(3)参加反应的HCl的物质的量:n(HCl)=______________。
练习册系列答案
相关题目
下列实验操作能达到实验目的的是(Cu-64 O-16 H-1 S-32) ( )
实验目的 | 实验操作 | |
A | 配制1.0mol/LCuSO4溶液 | 把25g胆矾晶体溶于水配成100mL溶液 |
B | 检验CaO中是否含有Ca(OH)2 | 可将其加水后滴加酚酞溶液 |
C | 实验制取大量CO2 | 向稀硫酸中加入大理石 |
D | 配制Fe(OH)3胶体 | 将饱和的FeCl3溶液滴加到热NaOH溶液中 |


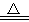 CO32-+NH3↑+2H2O
CO32-+NH3↑+2H2O 各组中所含的少量杂质(括号内为杂质),在空格中填上所需试剂的化学式:
各组中所含的少量杂质(括号内为杂质),在空格中填上所需试剂的化学式: