题目内容
1mol石膏(CaSO4?2H2O)加热到150℃,失去大部分结晶水变成熟石膏(2CaSO4?H2O),在此过程中失去结晶水的物质的量为( )
| A、2mol |
| B、1.5mol |
| C、1mol |
| D、0.5mol |
考点:化学方程式的有关计算,物质的量的相关计算
专题:计算题
分析:加热发生反应:2CaSO4?2H2O
2CaSO4?H2O+3H2O,根据方程式计算解答.
| ||
解答:
解:设失去结晶水的物质的量为n,则:
2CaSO4?2H2O
2CaSO4?H2O+3H2O
2 3
1mol n
所以n=
=1.5mol
故选B.
2CaSO4?2H2O
| ||
2 3
1mol n
所以n=
| 1mol×3 |
| 2 |
故选B.
点评:本题考查化学方程式有关计算,比较基础,也可以利用守恒守恒书写进行计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
已知:25℃H2C2O4 K1=5.4×10-2,K2=5.4×10-5;H2CO3 K1=4.5×10-7,K2=4.7×10-11;下列离子方程式一定不正确的是( )
| A、H2C2O4+CO32-=HCO3-+HC2O4- |
| B、HC2O4-+CO32-=HCO3-+C2O42- |
| C、H2C2O4+HCO3-=HC2O4-+H2O+CO2 |
| D、H2C2O4+CO32-=C2O42-+H2O+CO2 |
下列计算结果不正确的是( )
A、将标准状况下的a L氯化氢溶于1L水中.所得溶液的密度为d g/mL.则所得溶液的物质的量浓度为
| ||
| B、500mL氯化铁和氯化铜的混合溶液.其中含有0.2mol Fe3+和1.0mol的Cl-.其余是Cu2+,向其中加人足量的铁粉.充分反应后的溶液中含有Fe2+的物质的量为0.5mol | ||
| C、室温下,Mg(OH)2的Ksp=3.2×10-11.则室温时饱和Mg(OH)2溶液的pH=10.6 | ||
| D、一定量的CH4在不足量的氧气中燃烧,产生7.2g水,转移了1.4NA个电子.则燃烧产物中CO与CO2的物质的量之比为1:1 |
为了除去NO、NO2、NO2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理反应方程式:2NO2+2NaOH→NaNO3+NaNO2+H2O;NO2+NO+2NaOH→2NaNO2+H2O.现有由a mol NO、b mol NO2、c mol N2O4组成的混合气体恰好被V L氢氧化钠溶液吸收(无气体剩余).这次氢氧化钠溶液的物质的量浓度最小为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
化学与生活、生产密切相关,下列说法正确的是( )
| A、食盐、食醋、食用油均可用作食品添加剂,都属于有机物 |
| B、碳酸钡、碳酸氢钠、氢氧化铝均可作为抗酸药物使用 |
| C、工业生产玻璃和水泥,均需要用石灰石为原料 |
| D、海水淡化是解决淡水供应危机的方法之一,向海水中加入明矾可以使海水淡化 |
aA、bB、cC、dD、eE均为短周期元素.已知D与E同主族,其中d=
,c-l=
,c-d=
.下列说法正确的是( )
| e |
| 2 |
| d+e |
| 2 |
| b-a |
| 2 |
| A、原子半径:E>D>C |
| B、元素A与B一定同主族,且B为第3周期元素 |
| C、元素C的最高价氧化物属于碱性氧化物 |
| D、元素E的常见氧化物有2种,且它们之间可以相互转化 |
能正确表示下列反应的离子方程式是( )
| A、少量的CO2通人氨水中:CO2+NH3?H2O═NH4++HCO3- | ||||
| B、Na2O2溶于水中:2Na2O2+2H2O═4Na++4OH-+O2↑ | ||||
| C、钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-═Fe3+ | ||||
D、用惰性电极电解熔融氯化钠:2Cl-+2H2O
|
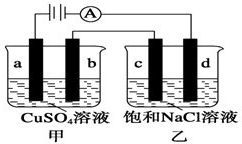 如图a、b、c、d均为石墨电极,通电进行电解(电解液足量).下列说法不正确的是( )
如图a、b、c、d均为石墨电极,通电进行电解(电解液足量).下列说法不正确的是( )| A、甲中a的电极反应式为4OH--4e-═O2↑+2H2O |
| B、向乙中加入适量盐酸,溶液组成可以恢复 |
| C、电解时向乙中滴入酚酞溶液,d电极附近先变红 |
| D、当b极有6.4g Cu析出时,c电极产生7.1g气体 |
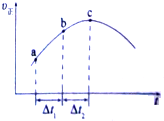 自一个恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g)?CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示.由此得出结论正确的是( )
自一个恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g)?CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示.由此得出结论正确的是( )| A、反应物浓度:a点小于c点 |
| B、△t1=△t2时氢气的产率:ab段小于bc段 |
| C、该反应的正反应为吸热反应 |
| D、c点反应进行的程度最大 |