题目内容
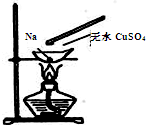 某学习资料上有这样一个实验:在蒸发皿中放黄豆粒大小的一块金属钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4粉末与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成.据此判断下列说法中不正确的是( )
某学习资料上有这样一个实验:在蒸发皿中放黄豆粒大小的一块金属钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4粉末与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成.据此判断下列说法中不正确的是( )| A、上述反应是置换反应 |
| B、上述反应是放热反应 |
| C、加热且无水条件下,Na可以与CuSO4反应并生成Cu |
| D、上述实验证明CuSO4具有还原性 |
考点:钠的化学性质
专题:金属概论与碱元素
分析:在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成,说明熔融的钠将硫酸铜中的铜置换出来并且放出热量,属于置换反应,钠作还原剂,硫酸铜作氧化剂,以此解答该题.
解答:
解:在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成,说明熔融的钠将硫酸铜中的铜置换出来并且放出热量,属于置换反应,钠作还原剂,硫酸铜作氧化剂,故选:D.
点评:本题考查钠的性质,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握题给信息,题目较好考查学生的自学能力,难度不大.

练习册系列答案
相关题目
下列说法不正确的是( )
①将BaSO4放入水中其溶液不能导电,所以BaSO4是非电解质
②氨溶于水得到的氨水能导电,所以氨水是电解质
③固态共价化合物不导电,熔融态的共价化合物可以导电
④固态离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
①将BaSO4放入水中其溶液不能导电,所以BaSO4是非电解质
②氨溶于水得到的氨水能导电,所以氨水是电解质
③固态共价化合物不导电,熔融态的共价化合物可以导电
④固态离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
| A、仅①④ | B、仅①④⑤ |
| C、仅①②③④ | D、①②③④⑤ |
甲苯苯环上的氢原子被两个溴原子取代,生成的二溴代物有6种,则甲苯苯环上的三溴代物有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
下列关于金属铝的叙述中,说法正确的是( )
| A、Al 是地壳中含量最多的元素 |
| B、Al 是比较活泼的金属,在化学反应中容易失去电子,表现氧化性 |
| C、Al箔在空气中受热可以熔化,且发生剧烈燃烧 |
| D、Al箔在空气中受热可以熔化,由于氧化膜的存在,熔化的Al 并不滴落 |
氢化钙可作为生氢剂,反应方程式为:CaH2+2H2O═Ca(OH)2+2H2↑,其中水的作用是( )
| A、溶剂 | B、还原剂 |
| C、氧化剂 | D、既作氧化剂,又作还原剂 |
下列化学用语正确的是( )
A、甲醛的电子式: |
B、异丙基的结构式: |
| C、甲醇的化学式:CH4O |
| D、乙醛的结构简式:CH3COH |
以下实验事实中能证明无色透明液体是纯净水的是( )
| A、测得该液体pH=7 |
| B、电解该液体得到氢气和氧气,测其体积比为2﹕1 |
| C、向其中投入金属钠,钠于液面上迅速游动,并发出嘶嘶声 |
| D、在1.01×105 Pa压强下测得沸点为373.15K |
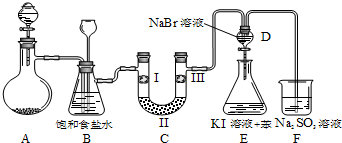
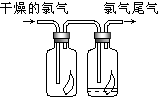 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是