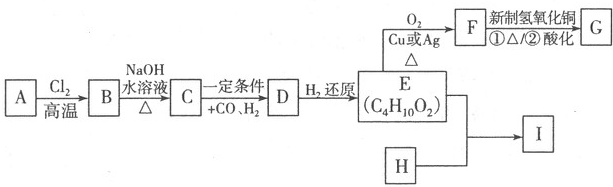
题目内容
某矿样含有大量的CuS、少量铁的氧化物及少量其它不溶于酸的杂质.某化学课外小组设计如图甲流程,以该矿样为原料生产CuCl2?2H2O晶体.
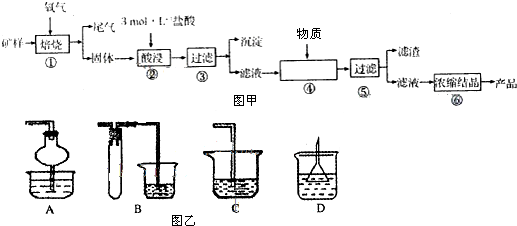
(1)在焙烧过程产生的尾气中,有一种是主要的大气污染物.若在实验室中以碱液吸收处理之,图乙装置可行的是 (填字母).
(2)步骤②酸浸过程中,需要用到3mol?L-1,的盐酸100mL,配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有 ;
(3)步骤④中,加入的X物质可以是 ,作用是 .

(1)在焙烧过程产生的尾气中,有一种是主要的大气污染物.若在实验室中以碱液吸收处理之,图乙装置可行的是
(2)步骤②酸浸过程中,需要用到3mol?L-1,的盐酸100mL,配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有
(3)步骤④中,加入的X物质可以是
考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:实验设计题
分析:(1)以碱液吸收处理的过程中主要是防止液体倒吸,根据装置的特点来选择即可;
(2)酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器依据配制溶液的步骤来选择即可;
(3)步骤④加入物质X的目的是控制溶液的PH,使Fe3+以沉淀的形式全部沉淀,物质X是和溶液中酸反应调节溶液PH,但不能引入新的杂质.
(2)酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器依据配制溶液的步骤来选择即可;
(3)步骤④加入物质X的目的是控制溶液的PH,使Fe3+以沉淀的形式全部沉淀,物质X是和溶液中酸反应调节溶液PH,但不能引入新的杂质.
解答:
解:矿样含有大量的CuS、少量铁的氧化物及少量其它不溶于酸的杂质,通入氧气,可以使硫化铜转化为含铜氧化物和二氧化硫气体,铜和铁的氧化物可以用盐酸来溶解,得到的溶液是氯化铜和氯化铁的混合物,过滤可以滤去不溶于酸的难溶物,对溶液加入一定的物质调节pH,可以将铁离子沉淀去,但是铜离子不沉淀,最终经过蒸发浓缩,冷却结晶,过滤、干洗涤、干燥,可以得到氯化铜晶体.
(1)在焙烧过程中还有废气产生,其中一种是主要的大气污染物.若在实验室中以碱液吸收处理之,处理过程中主要是防止液体倒吸,下列A、B、C装置中防倒吸的是AB,故答案为:AB;
(2)配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有100ml的容量瓶,量筒;故答案为:100ml的容量瓶,量筒;
(3)处理过程步骤④加入物质X的目的是控制溶液的PH,使Fe3+以沉淀的形式全部沉淀,物质X是和溶液中酸反应调节溶液PH,但不能引入新的杂质,所以可以选择氧化铜(或是碳酸铜、氢氧化铜、碱式碳酸铜等),
故答案为:氧化铜(或是碳酸铜、氢氧化铜、碱式碳酸铜等);调节溶液的PH,使Fe3+以沉淀的形式全部沉淀.
(1)在焙烧过程中还有废气产生,其中一种是主要的大气污染物.若在实验室中以碱液吸收处理之,处理过程中主要是防止液体倒吸,下列A、B、C装置中防倒吸的是AB,故答案为:AB;
(2)配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有100ml的容量瓶,量筒;故答案为:100ml的容量瓶,量筒;
(3)处理过程步骤④加入物质X的目的是控制溶液的PH,使Fe3+以沉淀的形式全部沉淀,物质X是和溶液中酸反应调节溶液PH,但不能引入新的杂质,所以可以选择氧化铜(或是碳酸铜、氢氧化铜、碱式碳酸铜等),
故答案为:氧化铜(或是碳酸铜、氢氧化铜、碱式碳酸铜等);调节溶液的PH,使Fe3+以沉淀的形式全部沉淀.
点评:本题考查了物质转化关系和物质性质的应用,主要考查物质分离的流程分析和原理利用,溶液配制,防倒吸的选择,难度中等.

练习册系列答案
相关题目
下列原子中,核外电子层数与最外层电子数互不相等的是( )
| A、H | B、Be | C、Mg | D、Al |
在下列所示的微粒中,氧化性最强的是( )
| A、1S22S22P2 |
| B、1S22S22P5 |
| C、1S22S22P63S1 |
| D、1S22S22P6 |
有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Ca2+、CO32-、SO42-,现取三份100mL溶液进行如下实验( )
(1)第一份加入AgNO3溶液由沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量2.33g.
(1)第一份加入AgNO3溶液由沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量2.33g.
| A、c(K+)≥0.2 mol/L |
| B、一定存在的离子:Cl- CO32-、SO42- NH4+ |
| C、一定不存在的离子:Ca2+ K+ Cl- |
| D、c(K+)+c(NH4+)=c(CO32-)+c(SO42-) |
下列实验中,金属或固体可以完全溶解的是( )
| A、在H2O2溶液中加入少量MnO2粉末 |
| B、镀锌铁皮加入足量的NaOH溶液中 |
| C、1mol铜片与含2mol H2SO4的浓硫酸共热 |
| D、常温下,1mol铜片投入含4mol HNO3的浓硝酸中 |
在核外电子排布如下的原子中,有最高化合价且其值最大的是( )
| A、1S22S22P2 |
| B、1S22S22P63S23P6 |
| C、1S22S22P5 |
| D、1S22S22P63S23P1 |
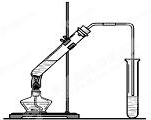 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: