题目内容
9.某同学参阅了“84消毒液”说明中的配方,欲用NaClO固体配制500mL含 NaClO 14.9%,密度为1.20g/cm3的消毒液.下列说法不正确的是( )| A. | 定容摇匀后,有少量溶液外流,则NaClO的物质的量浓度偏小 | |
| B. | 容量瓶用蒸馏水洗净后可以不烘干即能用于溶液的配制 | |
| C. | 所配得的NaClO消毒液在空气中光照,久置后溶液中NaClO的物质的量浓度减小 | |
| D. | 所配制NaClO溶液的物质的量浓度为2.4 mol•L-1 |
分析 A.根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
B.容量瓶中有水,对溶液的体积无影响;
C.由于NaClO易吸收空气中的H2O、CO2而变质,所以NaClO消毒液变质导致NaClO减少;
d.依据难度计算式子带入计算分析=$\frac{1000×ρ×w%}{M}$;
解答 解:A.若定容摇匀后有少量溶液外流,此时溶液的浓度已经均一而且确定,故对所配溶液的浓度无影响,故A错误;
B.容量瓶中有水,对溶液的体积无影响,所以经洗涤干净的容量瓶不必烘干后再使用,故B正确;
C.由于NaClO易吸收空气中的H2O、CO2而变质,所以NaClO消毒液变质导致NaClO减少,配制的溶液中溶质的物质的量减小,则溶液的物质的量浓度减小,故C正确;
D.c=$\frac{1000×ρ×w%}{M}$=$\frac{1000×1.20×14.9%}{74.5}$=2.4mol/L.故D正确;
故选A.
点评 本题主要考查溶液配制的步骤、仪器以及误差分析等,难度中等,注意计算溶质的质量,物质的量和溶质质量分数的换算方法.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
19.用NA表示阿伏加德罗常数.下列说法正确的是( )
| A. | 常温常压下,28g CO和N2的混合物含有的分子数为 NA | |
| B. | 标准状况下,1mol氦气中含有的核外电子数为4NA | |
| C. | 标准状况下,22.4 L 苯中含有的苯分子数是NA | |
| D. | 常温常压下,0.10 mol•L-1CH3COOH溶液中含有的H+数小于0.1NA |
20.下列实验操作中错误的是( )
| A. | 分液中,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 称量氢氧化钠固体时,将氢氧化钠固体放在垫有滤纸的托盘 | |
| C. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| D. | 称量时,砝码应放在托盘天平的右盘 |
17.下列事实不属于盐类水解应用的是( )
| A. | 明矾、氯化铁晶体常用于净水或消毒 | |
| B. | 实验室通常使用热的纯碱溶液去除油污 | |
| C. | 实验室配制FeCl3溶液时加入少量稀盐酸 | |
| D. | 加热稀醋酸溶液其pH稍有减少 |
14.利用如图所示装置模拟电解原理在工业生产上的应用,下列说法正确的是( )
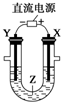

| A. | 氯碱工业中,X电极上反应式是4OH--4e-═2H2O+O2↑ | |
| B. | 电解精炼铜时,Z溶液中的Cu2+浓度不变 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 制取金属镁时,Z是熔融的氯化镁 |
18.下列离子方程式正确的是( )
| A. | 氯气与水反应:Cl2+H2O═Cl-+ClO-+2H+ | |
| B. | 铁与盐酸反应:2Fe+6H+═3H2↑+2Fe3+ | |
| C. | 硫酸与氢氧化钡混合:2H++SO42-+Ba2++2OH?═Ba SO4↓+2 H2O | |
| D. | 向AlCl3溶液中滴入过量NaOH溶液:Al3++3OH-=Al(OH)3↓ |