题目内容
12.氢气还原氧化铜:CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,该反应中( )| A. | H2作氧化剂 | B. | 铜元素化合价升高 | ||
| C. | 氢元素化合价降低 | D. | Cu是还原产物 |
分析 在氧化还原反应中失电子化合价升高的物质作还原剂,得电子化合价降低的物质作氧化剂,注意氧化剂、还原剂必须是反应物;反应CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O中Cu元素的化合价降低,H元素的化合价升高,以此来解答.
解答 解:A.该反应中,H元素化合价升高被氧化,氢气为还原剂,故A错误;
B.Cu元素化合价从+2变为0,铜元素化合价降低被还原,故B错误;
C.H元素从0价变为+1价,氢元素的化合价升高,故C错误;
D.CuO被氢气还原为Cu,则Cu是还原产物,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,题目难度不大.

练习册系列答案
相关题目
7.含有元素硒(Se)的保健品已经进入市场.已知硒元素与氧元素同主族,与钾元素同周期.下列关于硒的叙述不正确的是( )
| A. | 原子序数是34 | B. | 最高价氧化物的化学式为SeO3 | ||
| C. | 金属性比较强 | D. | 气态氢化物的化学式为H2Se |
8.同周期的四种短周期元素X、Y、Z和W的原子序数依次递增,其原子的最外层电子数之和为18,X和Y的原子序数比为6:7,X的最高正价是W的最低负价绝对值的2倍.下列说法正确的是( )
| A. | Y的氧化物不能与任何酸发生反应 | |
| B. | X和W可形成离子化合物 | |
| C. | X、Y、Z和W都没有同素异形体 | |
| D. | Z和W的最高价氧化物对应的水化物都是强酸 |
5.下列关于物质的量及粒子数的叙述,正确的是( )
| A. | 1 mol任何物质都含有6.02×1023个分子 | |
| B. | 0.012kg 12C中含有约6.02×1023个12C | |
| C. | 1mol CO2中含有1mol碳和2 mol氧 | |
| D. | 1mol H含有6.02×1024个质子 |
7.在一定温度下,将气体X和气体Y 各0.16mol充入10L 恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,反应过程中测定的数据如表( )
下列判断正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2min的平均速率v(Z)=2.0×10-3 mol/(L•min) | |
| B. | 其他条件不变,降低温度,平衡向正反应方向移动 | |
| C. | 当进行4分钟时,反应已达平衡状态 | |
| D. | 其他条件不变,通过缩小容器体积增大压强,平衡常数减小 |
17.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理正确的是( )
| 50ml盐酸 | 50ml盐酸 | 50ml盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
| A. | 15.7g混合物能恰好与盐酸完全反应 | |
| B. | 根据表中数据不能计算出混合物中NaHCO3的质量分数 | |
| C. | 向50ml盐酸中加入混合物27.6g时,盐酸过量 | |
| D. | 盐酸的物质的量浓度为3.0mol/L |
4.观察下列模型并结合相关信息,判断下列说法中不正确的是( )
| B12结构单元 | SF6 | S8 | HCN |
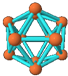 | 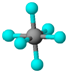 | 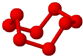 | 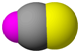 |
| 熔点1873K | 气体 | 易溶于CS2 | 溶液显弱酸性 |
| A. | 单质B12形成的晶体可能为原子晶体 | |
| B. | SF6是由极性键构成的非极性分子 | |
| C. | S8和HCN形成晶体后,晶体类型相同 | |
| D. | HCN形成晶体后,晶体中的作用力只有共价键 |
2.对于某些离子的检验方法(包括操作、现象、结论),完全正确的是( )
| A. | 向待测溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32- | |
| B. | 向待测溶液中逐滴加入氢氧化钠溶液,开始有白色沉淀生成,继续滴加氢氧化钠溶液到过量,沉淀逐渐溶解,一定有 Al3+ | |
| C. | 向待测溶液中先滴加盐酸酸化未出现沉淀,再加入 BaCl2 溶液有白色沉淀产生,一定有SO42- | |
| D. | 向待测溶液中滴加 NaOH 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,一定有NH4+ |
 某CuCl2溶液中可能混有盐酸,向该溶液中逐滴滴入某种碱溶液,产生沉淀的物质的量与加入碱的物质的量关系如图所示.据此推断:
某CuCl2溶液中可能混有盐酸,向该溶液中逐滴滴入某种碱溶液,产生沉淀的物质的量与加入碱的物质的量关系如图所示.据此推断: