题目内容
4.(1)某气态氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为64g/mol,R 的相对原子质量为32.(2)已知CO、CO2的混合气体质量共15g,标准状况下体积为8.8L,则可推知该混合气体中含CO4.2g.
(3)同温同压下,SO2与氢气的密度之比为32:1;若体积相同时,两种气体的质量比为32:1.
分析 (1)根据n=$\frac{V}{{V}_{m}}$、M=$\frac{m}{M}$计算出RO2的摩尔质量,然后结合化学式组成计算出R的相对原子质量;
(2)设出二者的物质的量,然后列式计算出CO的物质的量,然后根据m=nM计算出CO的质量;
(3)相同条件下,密度之比等于摩尔质量之比;相同条件下,体积相同的气体具有相同的物质的量,根据m=nM可知气体的质量与摩尔质量成正比.
解答 解:(1)标准状况下448mL 64g/mol气体的物质的量为:$\frac{0.448L}{22.4L/mol}$=0.02mol,该气体的摩尔质量为:$\frac{1.28g}{0.02mol}$=64g/mol;RO2的相对分子质量为64,则R的相对原子质量为:64-16×2=32,
故答案为:64g/mol;32;
(2)设混合气体中CO、CO2的物质的量分别为x、y,则:$\left\{\begin{array}{l}{28x+44y=15}\\{x+y=\frac{8.8L}{22.4L/mol}}\end{array}\right.$,解得:x=0.15mol、y=0.25mol
所以混合气体中CO的质量为:m(CO)=0.15mol×28g/mol=4.2g,
故答案为:4.2;
(3)相同条件下,密度之比等于摩尔质量之比,故SO2与氢气的密度之比=64g/mol:2g/mol=32:1;
若体积相同时,二者的物质的量相等,则两种气体的质量比=摩尔质量之比=64g/mol:2g/mol=32:1,
故答案为:32:1;32:1.
点评 本题考查了物质的量的计算,题目难度中等,明确物质的量与摩尔质量、气体摩尔体积之间的关系为解答关键,试题培养了学生的分析能力及化学计算能力.

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ③ | |||||||
| 3 | ① | ② | ④ | ⑤ | ||||
(2)④和⑤两种元素的最高价氧化物对应水化物酸性较弱的是H2SO4(填化学式),②和④两种元素中,原子半径较大的是Al(填元素符号).
(3)元素①的氢氧化物与元素②的单质反应,离子反应方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
| A. | m+n>p | B. | A 的转化率降低 | ||
| C. | 平衡向正反应方向移动 | D. | C的体积分数增加 |
| A. | p2<p1 | B. | p1<p2<2p 1 | C. | p1>2p2 | D. | 2p1=p2 |
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6、-2 | +5、-3 | -2 | +3 |
| A. | 离子半径大小:R3+<X+<M2- | |
| B. | Y与M组成的化合物是光化学烟雾的原因之一 | |
| C. | 将YM2通入Ba(NO3)2溶液中有大量白色沉淀产生 | |
| D. | R的单质是铝热剂的成分之一 |
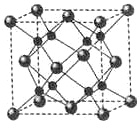 A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
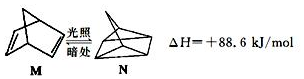
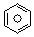 (l)的燃烧热为3267.5kJ•mol-1,
(l)的燃烧热为3267.5kJ•mol-1,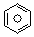 (l)+6O2(g)═6CO2(g)+3H2(g)
(l)+6O2(g)═6CO2(g)+3H2(g)