题目内容
20.已知某温度下,醋酸的电离常数K=1.6×10-5.计算0.010mol/L的醋酸溶液中,c(H+)是多少?分析 根据酸的电离常数计算H+浓度,K(醋酸)=$\frac{c(氢离子)×c(醋酸跟)}{c(醋酸)-c(氢离子)}$,由此分析解答.
解答 解:根据酸的电离常数,设电离的氢离子为xmol,列式:K=1.6×10-5=$\frac{x•x}{0.01-x}$,0.01-x≈0.01,解得x=4×10-4(mol/L),
答:c(H+)是4×10-4mol/L.
点评 本题考查根据电离平衡常数,结合电离方程式来求微粒氢离子的浓度,学生要清楚电离是极其微弱的,所以0.01-x≈0.01代入计算,比较容易.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列反应的离子方程式正确的是( )
| A. | 向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| B. | 向盐酸中滴加氨水:H++OH-═H2O | |
| C. | 金属钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 用FeCl3溶液腐蚀印刷电路铜板:Fe3++Cu═Fe2++Cu2+ |
11.下列物质属于电解质的是( )
| A. | NaCl | B. | CC14 | C. | Cu | D. | SO2 |
15.下列有关离子方程式与所述事实相符且正确的是( )
| A. | 过量的NaHSO4与Ba(OH)2溶液的反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| C. | 酸性条件下KIO3和KI溶液反应生成I2:IO3-+5I-+3H2O═3I2+6 OH- | |
| D. | Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
5.下列无色溶液能常量共存的离子组是( )
| A. | Ba2+、SO42-、Cl- | B. | K+、OH-、HCO3- | C. | Mg2+、SO42-、Cl- | D. | Cu2+、H+、Cl- |
12.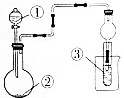 利用如图所示装置进行下列实验,不能得出相应实验结论的是( )
利用如图所示装置进行下列实验,不能得出相应实验结论的是( )
 利用如图所示装置进行下列实验,不能得出相应实验结论的是( )
利用如图所示装置进行下列实验,不能得出相应实验结论的是( )| 选项 | ① | ② | ③ | ③中的现象 |
| A | 浓盐酸 | Na2SO3 | BaCl2溶液 | 出现浑浊 |
| B | 稀盐酸 | 石灰石 | 饱和Na2CO3溶液 | 出现浑浊 |
| C | 浓氨水 | 生石灰 | 酚酞溶液 | 出现红色 |
| D | 醋酸 | 贝壳 | 澄清石灰水 | 先浑浊后澄清 |
| A. | A | B. | B | C. | C | D. | D |
17.今年“世界地球日”的主题是:“珍惜地球资源,转变发展方式,提高资源利用效益”,下列行为中不符合这一主题的是( )
| A. | 节约能源,提高能源利用率 | |
| B. | 大量开采化石原料,以满足社会对能源的要求 | |
| C. | 减少直至不使用对大气臭氧层起破坏作用的氟氯烃 | |
| D. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 |
18.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温下,28g CO中含有的分子数为NA | |
| B. | 1.0 mol•L-1 Na2SO4溶液中所含的Na+数为2NA | |
| C. | 标准状况下,22.4 L HCl气体中所含的原子数为NA | |
| D. | 1 mol N2所含有的原子数为NA |