题目内容
将1L含有0.4mol CuSO4和0.2mol NaCl的水溶液用惰性电极电解一段时间后,若在一个电极上得到0.3mol Cu,则:
求:(1)另一电极上析出气体(在标准状况下)的体积是多少?
(2)此时溶液的H+离子浓度是多少?(溶液体积变化不计)
求:(1)另一电极上析出气体(在标准状况下)的体积是多少?
(2)此时溶液的H+离子浓度是多少?(溶液体积变化不计)
考点:电解原理
专题:
分析:(1)电解硫酸铜和氯化钠溶液时,阳极上氯离子先放电,然后氢氧根离子放电,阴极上铜离子放电,后氢离子放电,当阴极上析出析出铜的物质的量为0.3mol<0.4mol,根据转移电子守恒计算阳极上生成气体体积;
(2)根据电极上电子转移为0.4mol,4OH--4e-=2H2O+O2↑,反应的氢氧根的物质的量就是氢离子的物质的量.
(2)根据电极上电子转移为0.4mol,4OH--4e-=2H2O+O2↑,反应的氢氧根的物质的量就是氢离子的物质的量.
解答:
解:(1)电解硫酸铜和氯化钠溶液时,阳极上氯离子先放电,然后氢氧根离子放电,阴极上铜离子放电,后氢离子放电,当阴极上析出析出铜的物质的量为0.3mol,阴极上转移电子的物质的量=0.3mol×2=0.6mol,
根据原子守恒知,溶液中n(Cl-)=0.2mol,氯离子完全放电时转移电子的物质的量=0.2mol×1=0.2mol,生成氯气0.1mol;
所以阳极上有氧气生成,电极上电子转移为0.4mol,4OH--4e-=2H2O+O2↑,电极反应计算生成氧气0.1mol,所以阳极生成气体物质的量为0.2mol,标准状况下气体的体积为4.48L,
答:另一电极上析出气体(在标准状况下)的体积是4.48L;
(2)根据电极上电子转移为0.4mol,4OH--4e-=2H2O+O2↑,反应的氢氧根的物质的量就是氢离子的物质的量=0.4mol.溶液的体积是1L,浓度为0.4mol.L-1,
答:此时溶液的H+离子浓度是0.4mol.L-1.
根据原子守恒知,溶液中n(Cl-)=0.2mol,氯离子完全放电时转移电子的物质的量=0.2mol×1=0.2mol,生成氯气0.1mol;
所以阳极上有氧气生成,电极上电子转移为0.4mol,4OH--4e-=2H2O+O2↑,电极反应计算生成氧气0.1mol,所以阳极生成气体物质的量为0.2mol,标准状况下气体的体积为4.48L,
答:另一电极上析出气体(在标准状况下)的体积是4.48L;
(2)根据电极上电子转移为0.4mol,4OH--4e-=2H2O+O2↑,反应的氢氧根的物质的量就是氢离子的物质的量=0.4mol.溶液的体积是1L,浓度为0.4mol.L-1,
答:此时溶液的H+离子浓度是0.4mol.L-1.
点评:本题以电解原理为载体考查了物质的量的有关计算,明确阳极上析出气体的成分再结合转移电子相等即可解答,题目难度中等.

练习册系列答案
相关题目
关于下列化学物质的说法,正确的是( )
| A、MgO和Al2O3在工业上均可用于制耐高温材料,也常用于电解法冶炼镁、铝两种金属 |
| B、因为沸点Na>K,所以反应Na+KCl=K+NaCl能进行,可以用Na制得K |
| C、化学性质很不活泼的元素,在自然界中可能存在游离态单质,如:Pt、Si等元素 |
| D、Fe是黑色金属,但纯铁是银白色的,而且纯铁比生铁更容易被腐蚀 |
向溴化铁溶液中加入足量新制氯水,将溶液蒸干并充分灼烧,最后得到的固体是( )
| A、Fe2O3 |
| B、FeCl3 |
| C、FeCl3和Br2 |
| D、Fe(OH)3 |
把下列溶液加水稀释,溶液中每种离子的浓度都不会增加的是( )
| A、CH3COOH溶液 |
| B、NaCl溶液 |
| C、NaOH溶液 |
| D、FeCl3溶液 |
2011年9 月29日,“长征-2F”运载火箭成功将“天宫一号”目标飞行器送上太空,火箭中使用的燃料是偏二甲肼(CH3-NH-NH-CH3)和四氧化二氮(N2O4).在火箭升空过程中,燃料发生反应:CH3-NH-NH-CH3+2N2O4→2CO2+3N2+4H2O提供能量.下列叙述正确的是( )
| A、该燃料绿色环保,在燃烧过程中不会造成任何环境污染 |
| B、该反应中N2O4是氧化剂,偏二甲肼是还原剂 |
| C、CO2是氧化产物,N2是还原产物 |
| D、每有0.6 mol N2生成,转移电子数目为2.4NA |
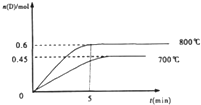 2L容积不变的密闭容器中,加入1.0molA和2.2molB,进行如下反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图,试回答下列问题:
2L容积不变的密闭容器中,加入1.0molA和2.2molB,进行如下反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图,试回答下列问题: