题目内容
11.我国预计在2020年前后建成自己的载人空间站.为了实现空间站的零排放,循环利用人体呼出的CO2并提供O2,我国科学家设计了一种装置(如图),实现了“太阳能一电能一化学能”转化,总反应方程式为2CO2=2CO+O2.关于该装置的下列说法不正确的是( )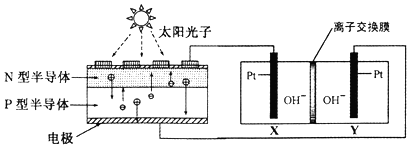
| A. | 图中N型半导体为负极,P型半导体为正极 | |
| B. | 图中离子交换膜为阴离子交换膜 | |
| C. | 反应完毕,该装置中电解质溶液的碱性增强 | |
| D. | 人体呼出的气体参与X电极的反应:CO2+2e一+H2O=CO+2OH- |
分析 装置实现“太阳能一电能一化学能”转化,电能转化为化学能,为电解装置,总反应为2CO2=2CO+O2,阴极发生还原反应生成CO,氧气发生氧化反应生成氧气,由电子的定向移动可知X为阴极,Y为阳极,以此解答该题.
解答 解:A、图中N型半导体为负极,P型半导体为正极,故A正确;
B、图中离子交换膜允许氢氧根离子通过,为阴离子交换膜,故B正确;
C.阴极反应生成的OH-在阳极完全反应,总反应为2CO2=2CO+O2,所以反应前后溶液的pH并不变化,故C错误;
D.人体呼出的气体参与X电极的反应:为CO2+H2O+2e-=CO+2OH-,故D正确.
故选C.
点评 本题考查化学电源新型电池,为高频考点,侧重于学生的分析能力的考查,明确负极反应=总反应-正极反应式是解答本题的关键,注意电解原理的应用,题目难度中等.

练习册系列答案
相关题目
1.下列微粒中,最外层电子数最多的是( )
| A. | Ne | B. | Al3+ | C. | Fe | D. | Fe2+ |
2.下列解释实验事实的化学方程式正确的是( )
| A. | FeCl3溶液中通入SO2,溶液黄色褪去:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| B. | 90℃时,测得纯水中c(H+)•c(OH-)=3.8×10-13:H2O(l?)H+(aq)+OH-(aq)△H<0 | |
| C. | 氨水中滴入酚酞溶液.溶液变红:NH3•H2O═NH4++OH- | |
| D. | 向澄清石灰水中通入过量CO2,溶液变浑浊:Ca2++CO2+2OH-═CaCO3↓+H2O |
19.下列说法不正确的是( )
| A. | 20℃时,AgCl固体在等物质的量浓度的NaCl、MgCl2溶液中的溶度积相同 | |
| B. | 浓度为0.2mol/L的KHCO3溶液:c(H2CO3)>c(CO32-) | |
| C. | a mol/LHCN溶液与b mol/L NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b | |
| D. | 常温下,在0.1mol/L的NaOH溶液中,由水电离出的c(H+)<$\sqrt{{K}_{W}}$ |
6.分子式满足C8H10的苯的同系物,一氯代物共有( )
| A. | 6 种 | B. | 9 种 | C. | 10 种 | D. | 14 种 |
3.已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )
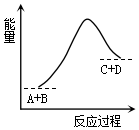

| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 该反应只有在加热条件下才能进行 | |
| C. | 该反应为放热反应 | |
| D. | 该反应为吸热反应 |
20.在A、B两个烧杯的溶液中,共含有Fe2+、Na+、H+、NO3-、Cl-、OH-6种离子,已知B烧杯为无色溶液,含有大量的其中三种离子,则A烧杯的溶液中含有大量的另外三种离子是( )
| A. | NO3-、OH-、Na+ | B. | Fe2+、H+、Cl- | C. | Fe2+、OH-、NO3- | D. | Fe2+、H+、NO3- |
20.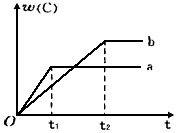 如图表示反应A(g)+B(g)?nC(g);△H<0,在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线.下列有关叙述正确的是( )
如图表示反应A(g)+B(g)?nC(g);△H<0,在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线.下列有关叙述正确的是( )
 如图表示反应A(g)+B(g)?nC(g);△H<0,在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线.下列有关叙述正确的是( )
如图表示反应A(g)+B(g)?nC(g);△H<0,在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线.下列有关叙述正确的是( )| A. | 反应起始由逆反应开始建立平衡 | |
| B. | a表示有催化剂,b表示无催化剂 | |
| C. | 若n=2,其它条件相同,a比b的压强大 | |
| D. | 若其它条件相同,a比b的温度高 |

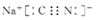 .
.