题目内容
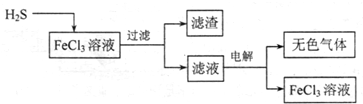
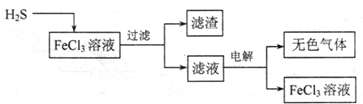
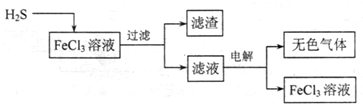
含硫化氢的工业废气要经过治理方能排放,既回收硫单质又防止大气污染.请根据如下治理方法回答相关问题.(1)电解法治理硫化氢的工艺流程如下:

①FeCl3溶液吸收H2S的生成物是______
②用惰性电极电解滤液时,阴极的电极反应式为______,电解总反应的离子方程式是______ 2Fe3++H 2↑
【答案】分析:(1)①三价铁具有氧化性,硫化氢具有还原性,二者之间发生氧化还原反应;
②电解氯化亚铁时,阴极发生得电子的还原反应,根据两极反应可写总的电解反应;
(2)①碳酸钠和硫化氢发生复分解反应,碳酸氢钠和强碱NaOH反应得到碳酸钠;
②硫化氢可以被氧气氧化为单质硫,根据硫化氢和氧气的量的关系以及氧气在空气中的含量进行计算;
(3)两种方法中氯化铁和碳酸钠可以循环使用.
解答:解:(1)①三价铁具有氧化性,硫化氢具有还原性,二者之间发生氧化还原反应,2FeCl3+3H2S=2FeCl2+6HCl+3S↓,故答案为:FeCl2、HCl和S(或答氯化亚铁、盐酸和硫单质);
②电解氯化亚铁时,阴极发生氢离子得电子的还原反应,2H++2e-═H 2↑,阳极亚铁离子发生失电子的氧化反应,2Fe2+═2Fe3++2e-,根据两极反应可写总的电解反应为:2Fe2++2H+ 2Fe3++H 2↑,故答案为:2H++2e-═H 2↑;2Fe2++2H+
2Fe3++H 2↑,故答案为:2H++2e-═H 2↑;2Fe2++2H+ 2Fe3++H 2↑;
2Fe3++H 2↑;
(2)①碳酸钠和硫化氢发生的反应为:CO32-+H2S═HS-+HCO3-,碳酸氢钠和强碱NaOH反应得到碳酸钠,
即HCO3-+OH-═CO32-+H 2O,故答案为:CO32-+H2S═HS-+HCO3-;HCO3-+OH-═CO32-+H 2O;
②硫化氢可以被氧气氧化为单质硫,根据硫化氢和氧气的量的关系2H 2S~O 2,消耗氧气的量10%×1800m3×0.5=90m3,氧气站空气含量的20%,所以理论上消耗空气的体积=90m3×5=450m3,故答案为:450;
(3)两种方法中氯化铁和碳酸钠可以循环使用,故答案为:吸收剂可循环使用.
点评:本题是一道有关物质性质的综合题目,思维空间广,难度较大.
②电解氯化亚铁时,阴极发生得电子的还原反应,根据两极反应可写总的电解反应;
(2)①碳酸钠和硫化氢发生复分解反应,碳酸氢钠和强碱NaOH反应得到碳酸钠;
②硫化氢可以被氧气氧化为单质硫,根据硫化氢和氧气的量的关系以及氧气在空气中的含量进行计算;
(3)两种方法中氯化铁和碳酸钠可以循环使用.
解答:解:(1)①三价铁具有氧化性,硫化氢具有还原性,二者之间发生氧化还原反应,2FeCl3+3H2S=2FeCl2+6HCl+3S↓,故答案为:FeCl2、HCl和S(或答氯化亚铁、盐酸和硫单质);
②电解氯化亚铁时,阴极发生氢离子得电子的还原反应,2H++2e-═H 2↑,阳极亚铁离子发生失电子的氧化反应,2Fe2+═2Fe3++2e-,根据两极反应可写总的电解反应为:2Fe2++2H+
 2Fe3++H 2↑,故答案为:2H++2e-═H 2↑;2Fe2++2H+
2Fe3++H 2↑,故答案为:2H++2e-═H 2↑;2Fe2++2H+ 2Fe3++H 2↑;
2Fe3++H 2↑;(2)①碳酸钠和硫化氢发生的反应为:CO32-+H2S═HS-+HCO3-,碳酸氢钠和强碱NaOH反应得到碳酸钠,
即HCO3-+OH-═CO32-+H 2O,故答案为:CO32-+H2S═HS-+HCO3-;HCO3-+OH-═CO32-+H 2O;
②硫化氢可以被氧气氧化为单质硫,根据硫化氢和氧气的量的关系2H 2S~O 2,消耗氧气的量10%×1800m3×0.5=90m3,氧气站空气含量的20%,所以理论上消耗空气的体积=90m3×5=450m3,故答案为:450;
(3)两种方法中氯化铁和碳酸钠可以循环使用,故答案为:吸收剂可循环使用.
点评:本题是一道有关物质性质的综合题目,思维空间广,难度较大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目