题目内容
6.如图表示吸热反应、置换反应、氧化还原反应之间的关系,下列反应中,属于Ⅴ区域的是( )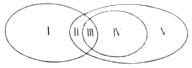
| A. | NaOH+HCl═NaCl+H2O | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | D. | 2Na+2H2O═2NaOH+H2↑ |
分析 置换反应一定属于氧化还原反应,由图可知Ⅰ为吸热反应,Ⅱ为吸热反应、氧化还原反应,Ⅲ为吸热反应、置换反应,Ⅳ为置换反应,Ⅴ为氧化还原反应,但不是吸热反应、置换反应,以此解答该题.
解答 解:A.NaOH+HCl═NaCl+H2O属于放热反应、非氧化还原反应,不在图中任何区域,故A错误;
B.2Na2O2+2H2O═4NaOH+O2↑属于放热反应,氧化还原反应,且不是置换反应,在Ⅴ区域,故B正确;
C.2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑属于吸热反应,非氧化还原反应,不在图中任何区域,故C错误;
D.2Na+2H2O═2NaOH+H2↑属于放热反应,置换反应,属于Ⅳ区,故D错误.
故选B.
点评 本题考查化学反应类型的判断,为高频考点,侧重考查学生的分析能力以及相关概念的理解,注意把握反应类型的判断,难度不大.

练习册系列答案
相关题目
16.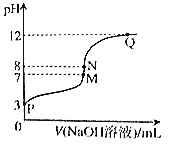 T℃时,在20.00mL0.10mol•L-1CH3COOH溶液中滴入0.10mol•L-1NaOH溶液,溶液pH与NaOH溶液体积关系关系如图所示.下列说法正确的是( )
T℃时,在20.00mL0.10mol•L-1CH3COOH溶液中滴入0.10mol•L-1NaOH溶液,溶液pH与NaOH溶液体积关系关系如图所示.下列说法正确的是( )
 T℃时,在20.00mL0.10mol•L-1CH3COOH溶液中滴入0.10mol•L-1NaOH溶液,溶液pH与NaOH溶液体积关系关系如图所示.下列说法正确的是( )
T℃时,在20.00mL0.10mol•L-1CH3COOH溶液中滴入0.10mol•L-1NaOH溶液,溶液pH与NaOH溶液体积关系关系如图所示.下列说法正确的是( )| A. | T℃时,CH3COOH电离平衡常数Ka=1.0×10-3 | |
| B. | M点对应的NaOH溶液体积为20.00mL | |
| C. | N点与Q点所示溶液中水的电离程度:N>Q | |
| D. | N点所示溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
17.某元素R的最高价氧化物的水化物分子式是H3RO4,则在气态氢化物中R元素的化合价是( )
| A. | -1 | B. | -2 | C. | -3 | D. | -4 |
1.短周期主族元素X、Y、Z、W的原子序数依次增大,Y、Z原子的电子数之比为3:4;X、Z、W三种元素可组成化合物甲,25℃时,0.1mol•L-1甲溶液的pH=13,下列说法正确的是( )
| A. | 简单离子半径:W>Z | |
| B. | X和W形成的化合物属于离子化合物 | |
| C. | 由X、Y、Z三种元素组成化合物的水溶液一定显酸性 | |
| D. | Z最简单氢化物分子间存在氢键,故其稳定性强于Y最简单氢化物 |
11.在相同的条件下,一定量的氢气在氧气中充分燃烧并放出热量.若生成液态水放出的热量为Q1;若生成气态水放出的热量为Q2.那么Q1与Q2之间的关系是( )
| A. | Q1>Q2 | B. | Q1<Q2 | C. | Q1=Q2 | D. | 无法确定 |
18.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将FeCl3溶液加入Mg(OH)2悬浊液中 | 观察到沉淀由白色变为红褐色 | Fe(OH)3的溶解度大于Mg(OH)2 |
| B | 向某溶液中滴加BaCl2溶液,随后加稀硝酸酸化 | 溶液中产生白色沉淀,加稀硝酸不溶解 | 原溶液中一定含有SO42- |
| C | 将稀硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中 | 溶液变黄色 | 氧化性:H2O2比Fe3+强 |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
4.下列实验方案设计中,能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 检验FeCl3溶液中是否存在FeCl2 | 向溶液中滴加KSCN溶液后再滴加氯水 |
| B | 证明H2CO3酸性比H2SiO3强 | Na2CO3和SiO2在高温下熔融反应 |
| C | 除去Cu粉中混有的CuO | 向混合物中滴加适量稀硫酸并过滤 |
| D | 检验未知溶液一定含有CO32- | 加入稀盐酸有无色无味的气体生成 |
| A. | A | B. | B | C. | C | D. | D |
5.在四个不同的容器中,在不同的条件下进行合成氨反应.根据下列在相同时间内测定的结果判断,生成氨气的速率最快的是( )
| A. | V(N2)=0.2 mol•L-1•min-1 | B. | V(H2)=0.1 mol•L-1•min-1 | ||
| C. | V(NH3)=0.15 mol•L-1•min-1 | D. | V(H2)=0.4 mol•L-1•min-1 |
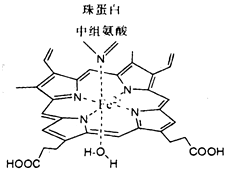 红细胞中血红素结构如图所示,回答下列问题:
红细胞中血红素结构如图所示,回答下列问题: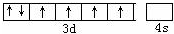 .
.