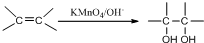题目内容
下列有关实验现象和解释或结论都正确的选项是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将电石与水反应产生的气体通入酸性高锰酸钾溶液 | 紫色褪去 | 证明有乙炔生成 |
| B | 将滴有酚酞的碳酸钠溶液加热 | 红色变深 | 水解过程是吸热的 |
| C | 把Cl2通入紫色石蕊试液中 | 紫色褪去 | Cl2具有漂白性 |
| D | 向碳酸钙粉末中滴加稀盐酸 | 有气泡产生 | 非金属性氯强于碳 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:
分析:A.电石不纯,与水反应生成乙炔的同时也生成硫化氢、磷化氢等;
B.升高温度促进水解;
C.氯气与水反应生成HCl、HClO,HClO具有漂白性;
D.应用最高价氧化物对应的水化物比较非金属性.
B.升高温度促进水解;
C.氯气与水反应生成HCl、HClO,HClO具有漂白性;
D.应用最高价氧化物对应的水化物比较非金属性.
解答:
解:A.电石不纯,与水反应生成乙炔的同时也生成硫化氢、磷化氢等,都可与高锰酸钾溶液反应,应先除杂,故A错误;
B.碳酸钠溶液中滴入酚酞试液,加热后若红色加深,则升高温度促进水解,即水解反应为吸热反应,故B正确;
C.氯气与水反应生成HCl、HClO,则氯气通入石蕊试液先变红后褪色,HClO具有漂白性,故C错误;
D.应用最高价氧化物对应的水化物比较非金属性,HCl是氢化物,不是最高价氧化物对应的水化物,故D错误.
故选B.
B.碳酸钠溶液中滴入酚酞试液,加热后若红色加深,则升高温度促进水解,即水解反应为吸热反应,故B正确;
C.氯气与水反应生成HCl、HClO,则氯气通入石蕊试液先变红后褪色,HClO具有漂白性,故C错误;
D.应用最高价氧化物对应的水化物比较非金属性,HCl是氢化物,不是最高价氧化物对应的水化物,故D错误.
故选B.
点评:本题考查较为综合,涉及物质的性质实验方案的设计等知识,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意相关知识的学习与积累,难度不大.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、0.1mol Cl2与足量NaOH溶液反应,转移电子的数目为0.2NA |
| B、0.1mol苯乙烯中含有碳碳双键的数目为0.4NA |
| C、标准状况下,11.2L乙醇中含有羟基的数目为0.5NA |
| D、4.6g由NO2和N2O4组成的混合物中含有氧原子的数目为0.2NA |
下列有关化学用语表示正确的是( )
A、氮气的电子式: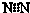 | ||
B、羟基的电子式: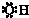 | ||
C、氯离子的结构示意图: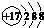 | ||
D、质子数为92、中子数为146的铀(U)原子的核素符号:
|
化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )
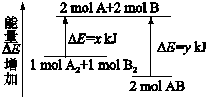

| A、该反应是吸热反应 |
| B、断裂2 mol A-B键需要吸收y kJ的能量 |
| C、2 mol AB的总能量高于1 mol A2和1 mol B2的总能量 |
| D、断裂1 mol A-A键和1 mol B-B键能放出x kJ的能量 |
一定量的混合气体,在密闭容器中发生如下反应:xA(g)+yB(g)?zC(g),达到平衡后测得A气体的浓度为2.5mol/L,当恒温下将密闭容器的容积缩小到原体积
时,再达到平衡后,测得A浓度为4.5mol/L,则下列叙述正确的是( )
| 1 |
| 2 |
| A、平衡向逆反应方向移动 |
| B、x+y<z |
| C、C的体积分数提高 |
| D、B的转化率降低 |
下列有关仪器使用方法或实验操作正确的是( )
| A、分液时下层液体从分液漏斗下端放出,上层液体从上口倒出 |
| B、酸碱滴定实验中,酸式滴定管装液前不必先用待装溶液润洗 |
| C、蒸馏过程中,冷却水从冷凝管的上端通入 |
| D、配制一定物质的量浓度的溶液时,直接将称取的固体药品倒入容量瓶加水溶解 |
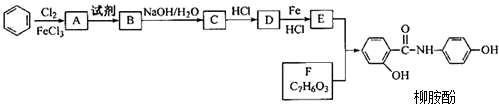
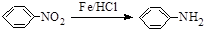 .请回答下列问题:
.请回答下列问题: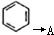 的化学方程式
的化学方程式