题目内容
7.工业上利用氢气在氯气中燃烧,所得产物再溶于水的方法制得盐酸,流程复杂且造成能量浪费.有人设想利用原电池原理直接制盐酸的同时,获取电能,假设这种想法可行,下列说法肯定错误的是( )| A. | 通入氢气的电极为原电池的正极 | |
| B. | 两极材料都用石墨,用稀盐酸做电解质溶液 | |
| C. | 电解质溶液中的阳离子向通氯气的电极移动 | |
| D. | 通氯气的电极反应式为Cl2+2e-═2Cl- |
分析 A、通氢气的电极发生失去电子的氧化反应;
B、根据原电池的工作原理知识是来判断;
C、原电池中电解质溶液中的阳离子向正极移动;
D、氯气发生得电子的还原反应.
解答 解:根据燃料电池的工作原理,利用原电池原理直接制盐酸的方程式为:H2+Cl2=2HCl,该原电池的工作原理和燃料电池的工作原理相似.
A、反应H2+Cl2=2HCl中,氢气失电子,所以通入氢气的电极为原电池的负极,故A错误;
B、两极材料可以都用石墨,一极通入氢气,一极通入氯气,可以用稀盐酸做电解质溶液,故B正确;
C、在原电池中,电解质溶液中的阳离子向正极移动,通氯气的电极为正极,故C正确;
D、通氯气的电极为正极,发生得电子得还原反应,电极反应式为:Cl2+2e-=2Cl-,故D正确.
故选A.
点评 本题考查学生原电池中燃料电池的工作原理知识,注意知识的迁移和应用,是一道信息迁移题目,难度不大.

练习册系列答案
相关题目
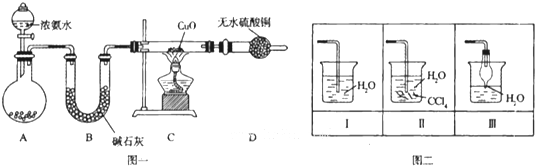
17.区别下列各组中的两种物质的方法错误的是( )
| A. | 甲烷和乙烯:分别通入酸性KMnO4溶液 | |
| B. | 苯和四氯化碳:分别与水混合、振荡、静置 | |
| C. | 乙醇和乙酸:分别滴加NaOH溶液 | |
| D. | 棉花织品和羊毛织品:分别燃烧闻气味 |
15.下列装置或操作能达到实验目的是( )
| A. | 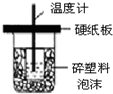 如图装置用于中和热的测定 | |
| B. | 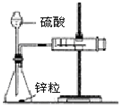 如图装置用于测定氢气的反应速率(单位mL/s) | |
| C. | 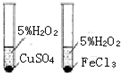 如图装置用于研究催化剂Cu2+和Fe3+对反应速率的影响 | |
| D. | 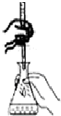 如图装置用于已知浓度的高锰酸钾溶液测定未知浓度的草酸溶液 |
8. 甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.
(1)该反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
设计实验方案如下(实验中所用MnSO4对该反应有催化作用):
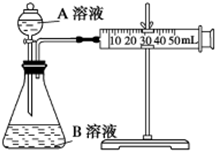
(2)甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小.实验装置如图,实验时分液漏斗中A溶液一次性放下,A、B的成分见表:
该实验探究的是浓度和催化剂对化学反应速率的影响.在反应停止之前,相同时间内针管中所得CO2的体积由大到小的顺序是③>②>①(用实验序号填空).
(3)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率的大小.取两支试管各加入2mL 0.1mol/L H2C2O4溶液,另取两支试管各加入4mL 0.1mol/L KMnO4溶液.将四支试管分成两组(各有一支盛有H2C2O4溶液和KMnO4溶液的试管),一组放入冷水中,另一组放入热水中,经过一段时间后,分别混合并振荡,记录溶液褪色所需时间.该实验目的是研究温度对化学反应速率的影响,但该组同学始终没有看到溶液褪色,其原因是没有加入稀硫酸酸化或高锰酸钾过量导致.
 甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.(1)该反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
设计实验方案如下(实验中所用MnSO4对该反应有催化作用):
(2)甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小.实验装置如图,实验时分液漏斗中A溶液一次性放下,A、B的成分见表:
| 序号 | A溶液 | B溶液 |
| ① | 2mL 0.1mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液 |
| ② | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液 |
| ③ | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液和少量MnSO4 |
(3)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率的大小.取两支试管各加入2mL 0.1mol/L H2C2O4溶液,另取两支试管各加入4mL 0.1mol/L KMnO4溶液.将四支试管分成两组(各有一支盛有H2C2O4溶液和KMnO4溶液的试管),一组放入冷水中,另一组放入热水中,经过一段时间后,分别混合并振荡,记录溶液褪色所需时间.该实验目的是研究温度对化学反应速率的影响,但该组同学始终没有看到溶液褪色,其原因是没有加入稀硫酸酸化或高锰酸钾过量导致.
9.如表所示的几种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法错误的是( )
| Q | X | Y | ||
| M | W | Z |
| A. | 相同条件下,Q元素最低价简单氢化物是同主族元素中氢化物沸点最高的 | |
| B. | 物质W3X4中,每个原子最外层均达到8电子稳定结构 | |
| C. | X、Q、Y和氢形成的化合物中可能既有离子键、又有共价键 | |
| D. | 将Q的最高价氧化物分别通入W的盐溶液和M的盐溶液中均可产生白色沉淀 |
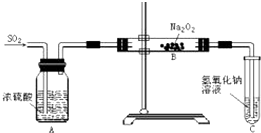 有两个实验小组的同学为探究过氧化钠与二氧化硫反应,都用如图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.
有两个实验小组的同学为探究过氧化钠与二氧化硫反应,都用如图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.