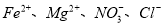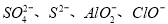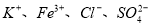题目内容
下述实验不能达到预期实验目的的是( )
序号 | 实验内容 | 实验目的 |
A | 将2.5gCuSO4·5H2O溶解在97.5g水中 | 配制质量分数为1.6%的CuSO4溶液 |
B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
C | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
C
【解析】
试题分析:A将2.5gCuSO4·5H2O溶解在97.5g水中,得到100g溶液,其中溶质CuSO4的质量是1.6g,所以可以配制质量分数为1.6%的CuSO4溶液,错误;A.向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液,会产生Ag2S沉淀是因为Ag2S溶度积产生效益AgCl,说明一种沉淀能转化为另一种溶解度更小的沉淀,正确;C.由于HClO有强氧化性,会把变色的pH试纸氧化,所以不能测定溶液的酸碱性,也就不能比较HClO和CH3COOH的酸性强弱,错误;D。室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸,根据沉淀测定的快慢来比较浓度对反应速率的影响,正确。
考点:考查化学实验操作与实验目的的关系的知识。

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目

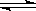 [Fe(SCN) ]2+ 。
[Fe(SCN) ]2+ 。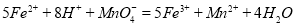 。准确称量上述药品10.00g,将其全部溶于试剂2中,配 制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
。准确称量上述药品10.00g,将其全部溶于试剂2中,配 制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
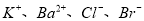
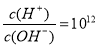 的溶液中:
的溶液中: