题目内容
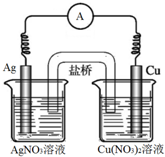 将反应Cu(s)+2Ag+(aq)?Cu2+(aq)+2Ag(s)设计成如下原电池,有关叙述正确的是( )
将反应Cu(s)+2Ag+(aq)?Cu2+(aq)+2Ag(s)设计成如下原电池,有关叙述正确的是( )| A、向硝酸银溶液中加入氯化钠固体,电流强度会减小 |
| B、向硝酸铜溶液中加入氢氧化钠固体,电流强度会减小 |
| C、将AgNO3溶液更换为Fe(NO3)3溶液,电流计指针偏转方向将相反 |
| D、当电流计指针为0时,该反应平衡常数K=0 |
考点:原电池和电解池的工作原理
专题:
分析:A、若此时向AgNO3溶液中加入NaCl固体,随着NaCl量的增加,Cl-与溶液中的Ag+形成AgCl沉淀,脱离溶液体系c(Ag+)逐渐减小,根据
和化学平衡常数的比值大小判断反应方向,当
>化学平衡常数时,反应向正反应方向移动,当
=化学平衡常数,反应达到平衡状态,当
<化学平衡常数
时,反应向逆反应方向移动;
B、向硝酸铜溶液中加入氢氧化钠固体时,氢氧化钠和硝酸铜反应生成氢氧化铜沉淀,根据
与化学平衡常数K′比较确定反应方向;
C、将AgNO3溶液更换为Fe(NO3)3溶液,只在左边的烧杯中发生反应;
D、当电流计指针为0时,该反应达平衡,但平衡常数K不等于0.
| [Ag+]2 |
| [Cu2+] |
| [Ag+]2 |
| [Cu2+] |
| [Ag+]2 |
| [Cu2+] |
| [Ag+]2 |
| [Cu2+] |
时,反应向逆反应方向移动;
B、向硝酸铜溶液中加入氢氧化钠固体时,氢氧化钠和硝酸铜反应生成氢氧化铜沉淀,根据
| [Cu2+] |
| [Ag+]2 |
C、将AgNO3溶液更换为Fe(NO3)3溶液,只在左边的烧杯中发生反应;
D、当电流计指针为0时,该反应达平衡,但平衡常数K不等于0.
解答:
解:A、若此时向AgNO3溶液中加入NaCl固体,随着NaCl量的增加,Cl-与溶液中的Ag+形成AgCl沉淀,脱离溶液体系c(Ag+)逐渐减小,
<化学平衡常数
时,反应向逆反应方向移动,电流强度减小,故A正确;
B、向Cu(NO3)2溶液中加入NaOH固体,氢氧化钠和硝酸铜反应生成氢氧化铜沉淀,铜离子浓度减小,
>化学平衡常数,反应向正反应方向移动,电流强度增大,故B错误;
C、将AgNO3溶液更换为Fe(NO3)3溶液,只在左边的烧杯中发生反应,不能形成原电池,故C错误;
D、当
=化学平衡常数,电流计指针为0,该反应达平衡,但平衡常数K不等于0,故D错误;
故选A.
| [Ag+]2 |
| [Cu2+] |
时,反应向逆反应方向移动,电流强度减小,故A正确;
B、向Cu(NO3)2溶液中加入NaOH固体,氢氧化钠和硝酸铜反应生成氢氧化铜沉淀,铜离子浓度减小,
| [Ag+]2 |
| [Cu2+] |
C、将AgNO3溶液更换为Fe(NO3)3溶液,只在左边的烧杯中发生反应,不能形成原电池,故C错误;
D、当
| [Ag+]2 |
| [Cu2+] |
故选A.
点评:本题考查原电池原理及化学平衡,明确指针的偏转幅度含义是解本题关键,知道K与
的差距越大,反应速度越快,难度中等.
| [Ag+]2 |
| [Cu2+] |

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
有四位同学分别对四种溶液中所含的离子进行检测,所得结果如下,其中所得结果错误的是( )
| A、Mg+、Na+、Cl-、NO3- |
| B、OH-、CO32-、Cl-、K+ |
| C、Cu2+、NO3-、OH-、Cl- |
| D、Ba2+、Na+、OH-、NO3- |
下列离子检验的方法正确的是( )
A、某溶液
| ||
B、某溶液
| ||
C、某溶液
| ||
D、某溶液
|
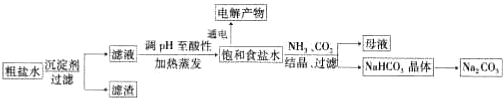
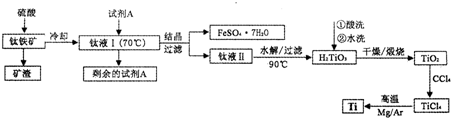
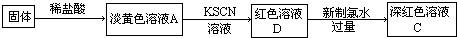
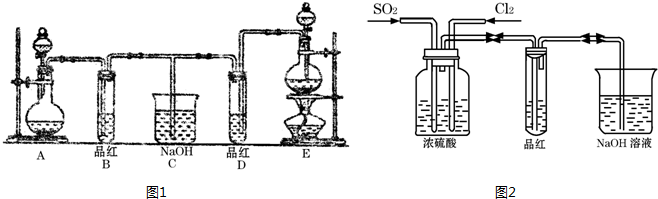

 ,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题:
,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题: