题目内容
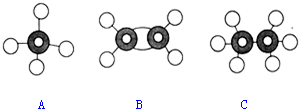
7.若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化.在变化的各阶段被破坏的粒子间的主要相互作用依次是( )| A. | 氢键 分子间作用力 非极性键 | B. | 氢键 氢键 极性键 | ||
| C. | 氢键 极性键 分子间作用力 | D. | 分子间作用力 氢键 非极性键 |
分析 根据雪花→水→水蒸气的过程为物理变化,破坏的是分子间作用力,主要是氢键,水蒸气→氧气和氢气是化学变化,破坏的是化学键,为极性键.
解答 解:固态水中和液态水中含有氢键,当雪花→水→水蒸气主要是氢键被破坏,但属于物理变化,共价键没有破坏,水蒸气→氧气和氢气,为化学变化,破坏的是极性共价键,
故选:B.
点评 本题考查氢键以及共价键,题目难度不大,要注意物质发生变化时粒子间的主要相互作用被破坏.

练习册系列答案
相关题目
15.下列说法不正确的是( )
| A. | 有些活泼金属如钠、镁、铝可作热还原法的还原剂 | |
| B. | 用电解熔融NaCl的方法来冶炼金属钠 | |
| C. | 回收废旧金属可以重新制成金属或它们的化合物 | |
| D. | 可用焦炭或一氧化碳还原氧化铝的方法来冶炼铝 |
2.实验室区别下列物质选用的试剂(括号中的为试剂,必要时可加热)正确的是( )
| A. | 苯和己烷(溴水) | B. | 矿物油和植物油(NaOH溶液) | ||
| C. | 乙醛和丙烯酸(KMnO4溶液) | D. | 硝基苯和CCl4(水) |
12.某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.
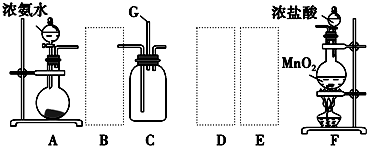
请回答下列问题:
(1)装置F中发生反应的离子方程式:MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O.
(2)装置A中的烧瓶内固体可选用ABE(选填以下选项的代号).
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择,并将编号填入下列空格:
BⅠ,DⅡ,EⅢ.(均填编号)
(4)从装置C的出气管口处逸出的尾气可能含有污染环境的有毒气体,如何处理?氢氧化钠溶液吸收.原理是(用化学方程式表示):Cl2+2NaOH=NaCl+NaClO+H2O.

| Ⅰ | Ⅱ | Ⅲ | |
| 备选装置 |  | 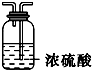 | 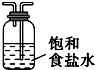 |
(1)装置F中发生反应的离子方程式:MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O.
(2)装置A中的烧瓶内固体可选用ABE(选填以下选项的代号).
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择,并将编号填入下列空格:
BⅠ,DⅡ,EⅢ.(均填编号)
(4)从装置C的出气管口处逸出的尾气可能含有污染环境的有毒气体,如何处理?氢氧化钠溶液吸收.原理是(用化学方程式表示):Cl2+2NaOH=NaCl+NaClO+H2O.
19.合成氨工业对国民经济和社会发展具有重要的意义.哈伯法合成氨需要在20-50MPa的高压和500℃的高温下,并用铁作为催化剂,氨的转化率为10%-15%.最近美国俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)2的催化剂,在常温下合成出氨,反应方程式可表示为N2+3H2→2NH3,有关说法正确的是( )
| A. | 哈伯法合成氨是吸热反应,新法合成氨是放热反应 | |
| B. | 新法合成和哈伯法相比不需要在高温条件下,可节约大量能源,具有发展前景 | |
| C. | 新法合成能在常温下进行是因为不需要断裂化学键 | |
| D. | 新的催化剂升高了反应所需要的能量,提高了活化分子百分数 |