题目内容
分析城市空气样本,主要污染物为可吸入颗粒物pm2.5、NOx、SO2等,其主要来源为燃煤和机动车尾气排放等。
(1) 某同学为检测样本中所含成份,将样本用蒸馏水处理制成待测试样,设计实验及实验现象如下:
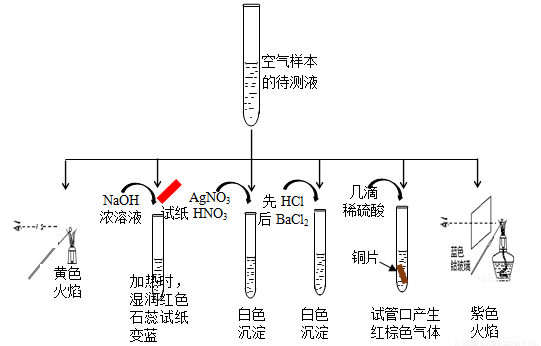
①该实验能确认存在的阳离子是 。
②该实验检测出样本中有NO3-,根据是(用化学方程式解释) 。
③根据该实验能否确定样本中含有SO32-, (填“能”或“否”) ,若要确定SO32-,所需的实验药品可以是 。
(2)PM2.5是指大气中直径小于或等于2.5μm(1μm =103 nm)的颗粒物。下列说法不正确的是 (填字母序号)。
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1 ~2.5μm的颗粒物分散到 空气中可形成胶体
空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(3)科研工作者用五年时间研究出利用石灰乳除工业燃煤尾气中的硫(SO2、SO3)和氮(NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4和Ca(NO2)2。
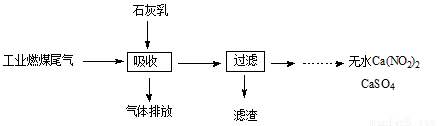
①CaSO4可以调节水泥的硬化时间。尾气中SO2与石灰乳反应生成CaSO4的化学方程式为 。
②Ca(NO2)2可制成混凝土防冻剂、钢筋阻锈剂等。尾气中NO、NO2与石灰乳反应生成Ca(NO2)2的化学方程式 。
练习册系列答案
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
反应:MgSO4(s) + CO(g) MgO(s)+CO2(g)+SO2(g) ΔH>0。在恒
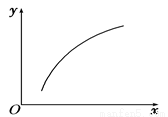
MgO(s)+CO2(g)+SO2(g) ΔH>0。在恒 容密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,y随x变化趋势合理的是
容密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,y随x变化趋势合理的是
选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |


 mol·L?1 B.
mol·L?1 B.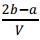 mol·L?1 C.
mol·L?1 C.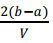 mol·L?1 D.
mol·L?1 D.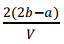 mol·L?1
mol·L?1 H++CH3COO-,下列叙述正确的是( )
H++CH3COO-,下列叙述正确的是( )
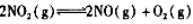

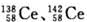 是同素异形体
是同素异形体 % B.25% C.50% D.75%
% B.25% C.50% D.75%