题目内容
下列分离、提纯、鉴别物质的方法正确的是( )
| A、用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| B、用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 |
| C、用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |
| D、用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
考点:物质的检验和鉴别的基本方法选择及应用,物质的分离、提纯和除杂
专题:物质检验鉴别题,化学实验基本操作
分析:A.BaSO4、BaCO3均不溶于水;
B.胶体可透过滤纸;
C.胶体具有丁达尔现象,而溶液不具有;
D.CaCl2、MgCl2杂质均溶于水.
B.胶体可透过滤纸;
C.胶体具有丁达尔现象,而溶液不具有;
D.CaCl2、MgCl2杂质均溶于水.
解答:
解:A.BaSO4、BaCO3均不溶于水,则溶解、过滤不能除杂,应加硫酸溶解后过滤除杂,故A错误;
B.胶体可透过滤纸,但淀粉胶体不能透过半透膜,而NaCl溶液可以,则用渗析的方法除去NaCl溶液中含有的少量淀粉胶体,故B错误;
C.胶体具有丁达尔现象,而溶液不具有,则丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液,故C正确;
D.CaCl2、MgCl2杂质均溶于水,则加热蒸发不能除杂,应利用沉淀法除杂,故D错误.
故选C.
B.胶体可透过滤纸,但淀粉胶体不能透过半透膜,而NaCl溶液可以,则用渗析的方法除去NaCl溶液中含有的少量淀粉胶体,故B错误;
C.胶体具有丁达尔现象,而溶液不具有,则丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液,故C正确;
D.CaCl2、MgCl2杂质均溶于水,则加热蒸发不能除杂,应利用沉淀法除杂,故D错误.
故选C.
点评:本题考查物质鉴别和检验,为高频考点,把握物质的性质及混合物分离提纯方法为解答的关键,侧重鉴别及除杂的考查,题目难度不大.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
高温下,超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价.如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是( )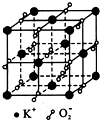

| A、超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2- |
| B、晶体中每个K+周围有8个O2-,每个O2-周围有8个K+ |
| C、晶体中与每个K+距离最近的K+有8个 |
| D、晶体中,0价氧原子与-2价氧原子的数目比为1:1 |
 I2在KI溶液中存在下列平衡:I2(aq)+I- (aq)?I3- (aq).某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I- (aq)?I3- (aq).某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法正确的是( )| A、反应 I2(aq)+I- (aq)?I3- (aq)的△H>0 |
| B、若温度为T1、T2,反应的平衡常数分别为K1、K2则K1>K2 |
| C、若反应进行到状态D时,一定有υ正<υ逆 |
| D、状态A与状态B相比,状态A的c(I2)大 |
某气态烃1mol能和2mol Br2加成,其饱和产物又能和6mol Cl2完全取代,则该烃是( )
| A、C2H6 |
| B、C4H6 |
| C、C3H4 |
| D、C2H2 |
能够用来鉴别BaCl2、NaCl、Na2CO3三种溶液的试剂是( )
| A、硝酸银溶液 | B、硫酸氢钠溶液 |
| C、稀盐酸 | D、稀硝酸 |
将Fe和Cu的质量比为7:8的混和粉末加入到200mL 4mol/L稀硝酸中充分反应(假定还原产物只有NO),则使HNO3完全反应的金属粉末的最小质量为( )
| A、12.0g |
| B、12.8g |
| C、14.4g |
| D、15.6g |
甲烷和丙烷以等体积混合其体积为V L,完全燃烧时所需氧气的体积(同温同压)是( )
| A、1.25V L |
| B、2.25V L |
| C、2.5V L |
| D、3.5V L |
向一由Fe、Cu组成的混合粉末中加入一定量的稀硝酸,充分反应后剩余金属X g,再各其中加入一定量的稀硫酸,充分振荡后余下金属Y g.则x和y之间的关系是( )
| A、X一定大于Y |
| B、X可能等于Y |
| C、X可能小于Y |
| D、X可能大于Y |
MgCl2溶液与Na2SO4溶液混和后,c(Mg2+)=c(SO42-),则下列说法不正确的是( )
| A、混和液中c(Cl-)=c(Na+) |
| B、混和液中c(Cl-)=2c(SO42-) |
| C、混和前两溶液体积相等 |
| D、混和前两溶液中MgCl2与Na2SO4物质的量相等 |