题目内容
16.下列递变规律正确的是( )| A. | HClO4、H2SO4、H3PO4的酸性依次增强 | |
| B. | HCl、HBr、HI的稳定性依次减弱 | |
| C. | 钠、镁、铝的还原性依次减弱 | |
| D. | P、S、Cl最高正化合价依次降低 |
分析 A.非金属性越强,对应最高价含氧酸的酸性越强;
B.非金属性越强,对应氢化物越稳定;
C.同周期从左向右金属性减弱;
D.第三周期从左向右最高正价增大,最外层电子数等于最高正价数.
解答 解:A.非金属性Cl>S>P,HClO4、H2SO4、H3PO4的酸性依次减弱,故A错误;
B.非金属性Cl>Br>I,HCl、HBr、HI的稳定性依次减弱,故B正确;
C.同周期从左向右金属性减弱,则钠、镁、铝的还原性依次减弱,故C正确;
D.第三周期从左向右最高正价增大,最外层电子数等于最高正价数,则P、S、Cl最高正化合价依次增大,故D错误;
故选BC.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
6.某透明溶液中,能大量共存的离子组是( )
| A. | Na+、Cu2+、Clˉ、SO42- | B. | Ca2+、K+、CO32ˉ、NO3ˉ | ||
| C. | Na+、H+、Clˉ、CO32ˉ | D. | K+、H+、Fe2+、NO3ˉ |
7.现有部分短周期主族元素的性质或原子结构如表:
(1)元素Z在周期表中的位置第3周期VⅡA族,XN2的结构式是:O=C=O,
(2)元素X的一种核素可测定文物年代,这种核素的符号是14C
(3)在X、Y最低价的简单氢化物中,较稳定的化合物的分子式是NH3.
(4)将少量W2N2固体投入到水中,剧烈反应,其反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑.
(5)下列表述中,能证明元素Z与元素T非金属性的强弱的是B
A、常温下Z的单质和T的单质状态不同
B、Z的氢化物比T的氢化物稳定
C、一定条件下Z和T的单质都能与氢氧化钠溶液反应.
| 元素符号 | 原子结构和元素性质 |
| T | M层上有6个电子 |
| W | 短周期内原子半径最大 |
| N | 原子序数比T小,且与T同主族 |
| X | 最外层电子数是次外层的2倍 |
| Y | 常见单质为双原子分子且氢化物的水溶液呈碱性 |
| Z | 元素最高价为+7 |
(2)元素X的一种核素可测定文物年代,这种核素的符号是14C
(3)在X、Y最低价的简单氢化物中,较稳定的化合物的分子式是NH3.
(4)将少量W2N2固体投入到水中,剧烈反应,其反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑.
(5)下列表述中,能证明元素Z与元素T非金属性的强弱的是B
A、常温下Z的单质和T的单质状态不同
B、Z的氢化物比T的氢化物稳定
C、一定条件下Z和T的单质都能与氢氧化钠溶液反应.
4.下列除杂的方法正确是( )
| A. | 除去CO2中的少量HCl:通入NaOH溶液,收集气体 | |
| B. | 除去H2中的少量HCl:通入Na2CO3溶液,收集气体 | |
| C. | 除去NaCl溶液中少量CaCl2:加入过量Na2CO3溶液,过滤 | |
| D. | 除去MgO中少量Al2O3:加入过量NaOH溶液,过滤 |
1. 乙烯催化氧化成乙酸可设计成如图所示的燃料电池,其总反应为:2CH2═CH2+O2→2CH3CHO.下列有关说法正确的是( )
乙烯催化氧化成乙酸可设计成如图所示的燃料电池,其总反应为:2CH2═CH2+O2→2CH3CHO.下列有关说法正确的是( )
 乙烯催化氧化成乙酸可设计成如图所示的燃料电池,其总反应为:2CH2═CH2+O2→2CH3CHO.下列有关说法正确的是( )
乙烯催化氧化成乙酸可设计成如图所示的燃料电池,其总反应为:2CH2═CH2+O2→2CH3CHO.下列有关说法正确的是( )| A. | 该装置能量转化形式是电能转化为化学能 | |
| B. | 负极反应式为:CH2═CH2+2e-+H2O═CH3CHO+2H+ | |
| C. | 每有0.1molO2反应,则向正极迁移的H+的物质的量为0.4mol | |
| D. | 电流方向:电极a→负载→电极b |
8. 瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.
瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.
下列有关叙述正确的是( )
 瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.
瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )
| A. | 电极a的反应式为:CH4+4O2--8e-=CO2+2H2O | |
| B. | 电极b是正极,O2-由电极a流向电极b | |
| C. | 瓦斯分析仪工作时,电池内电路中电子由电极 a流向电极b | |
| D. | 当固体电解质中有2 mol O2-通过时,外电路通过电子8 mol |
5.有3mL甲烷和一氧化碳的混合气体,完全燃烧恰好用去3mL氧气,则此混合气体中甲烷和一氧化碳的体积比是( )
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 任意比 |
 ;
; ,写出C2B2与A2B反应的离子方程式2Na2O2+2H2O═4Na++4OH-+O2↑;
,写出C2B2与A2B反应的离子方程式2Na2O2+2H2O═4Na++4OH-+O2↑;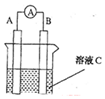 (1)如图所示,若C为浓硝酸,电流表指针发生偏转,B电极材料为Fe,A电极材料为Cu,则B电极的电极反应式为4H++2NO3-+2e-=2NO2↑+2H2O,A电极的电极反应式为Cu-2e-=Cu2+;反应进行一段时间后溶液C的pH将升高(填“升高”“降低”或“基本不变”).
(1)如图所示,若C为浓硝酸,电流表指针发生偏转,B电极材料为Fe,A电极材料为Cu,则B电极的电极反应式为4H++2NO3-+2e-=2NO2↑+2H2O,A电极的电极反应式为Cu-2e-=Cu2+;反应进行一段时间后溶液C的pH将升高(填“升高”“降低”或“基本不变”).