题目内容
8.硼镁泥是硼镁矿生产硼砂(Na2B4O7•lOH2O)时的废渣,其主要成分是Mg0,还含有CaO、Al2O3、Fe2O3、FeO、MnO、B2O3、SiO2等杂质.以硼镁泥为原料制取的七水硫酸镁在印染、造纸和医药等工业上都有广泛的应用.硼镁泥制取七水硫酸镁的工艺流程如下: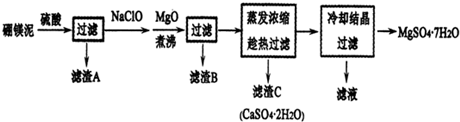
(1)滤渣A能溶于氢氟酸,写出其反应的化学方程式SiO2+4HF=SiF4↑+2H2O
(2)滤渣B中含有不溶于稀盐酸的黑色固体,则滤渣B含有的成分有Fe(OH)3、Al(OH)3、MnO2,加MgO并煮沸的目的是调节pH,促进Al3+、Fe3+完全水解生成氢氧化物沉淀而除去
(3)写出加NaClO过程中发生反应的离子方程式Mn2++ClO-+H2O═MnO2↓+2H++Cl-;2Fe2++ClO-+2H+═2Fe3++Cl-+H2O
(4)趁热过滤的目的是防止硫酸镁在温度降低时结晶析出
(5)因B2O3溶于硫酸,所以此法制备的七水硫酸镁含有少量硼酸(H3BO3),硼酸与NaOH溶液反应可制得硼砂,写出该反应的化学方程式4H3BO3+2NaOH+3H2O=Na2B4O7•lOH2O.失去结晶水的硼砂与金属钠、氢气及石英砂一起反应可制备有机化学中的“万能还原剂--NaBH4”和另一种钠盐,写出其反应的化学方程式Na2B4O7•lOH2O+16Na+8H2+7SiO2=4NaBH4+7Na2SiO3.
分析 硼镁泥主要成份是MgO,还有CaO、Al2O3、Fe2O3、FeO、MnO、B2O3、SiO2等杂质,加入硫酸,MgO、CaO、Al2O3、Fe2O3、FeO、MnO、B2O3都和硫酸反应,SiO2不与硫酸反应,次氯酸钠具有强氧化性,加入的NaClO可与Mn2+反应生成MnO2,把亚铁离子氧化成铁离子,加MgO调节pH,溶液pH升高,铁离子生成氢氧化铁沉淀,铝离子形成氢氧化铝沉淀,过滤,滤渣B含有Fe(OH)3、Al(OH)3、MnO2,蒸发浓缩滤液,趁热过滤,滤渣C为硫酸钙晶体,滤液中含镁离子,除钙后,只剩镁离子,蒸发冷却结晶得到硫酸镁晶体.
(1)二氧化硅与氢氟酸反应生成四氟化硅和水;
(2)根据流程分析判断;加MgO调节pH除去铁离子和铝离子;
(3)NaClO溶液在加热条件下将溶液中的Mn2+氧化成MnO2,溶液中含有Fe2+,具有还原性,可与NaClO发生氧化还原反应;
(4)温度较高时硫酸镁不会析出;
(5)H3BO3与NaOH溶液反应生成Na2B4O7•lOH2O;Na2B4O7•lOH2O与金属钠、氢气及二氧化硅反应生成NaBH4和硅酸钠.
解答 解:(1)滤渣A的成分是二氧化硅,二氧化硅与氢氟酸反应生成四氟化硅和水,其反应方程式为:SiO2+4HF=SiF4↑+2H2O;
故答案为:SiO2+4HF=SiF4↑+2H2O;
(2)由流程分析可知,滤渣B含有的成分有Fe(OH)3、Al(OH)3、MnO2;加MgO调节pH,铁离子水解生成氢氧化铁沉淀,铝离子水解形成氢氧化铝沉淀,从而除去溶液中的铁离子和铝离子;
故答案为:Fe(OH)3、Al(OH)3、MnO2;调节pH,促进Al3+、Fe3+完全水解生成氢氧化物沉淀而除去;
(3)NaClO溶液在加热条件下将溶液中的Mn2+氧化成MnO2,反应的离子方程式为Mn2++ClO-+H2O=MnO2↓+2H++Cl-,溶液中含有Fe2+,具有还原性,可与NaClO发生氧化还原反应,反应的离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+H2O,
故答案为:Mn2++ClO-+H2O═MnO2↓+2H++Cl-;2Fe2++ClO-+2H+═2Fe3++Cl-+H2O;
(4)温度较高时硫酸镁溶解度较大,硫酸钙的溶解度较小,温度越高,硫酸钙溶解度越小,可以采用蒸发浓缩,趁热过滤方法除去硫酸钙,可以防止硫酸镁在温度降低时结晶析出;
故答案为:防止硫酸镁在温度降低时结晶析出;
(5)H3BO3与NaOH溶液反应生成Na2B4O7•lOH2O,其反应方程式为:4H3BO3+2NaOH+3H2O=Na2B4O7•lOH2O;Na2B4O7•lOH2O与金属钠、氢气及二氧化硅反应生成NaBH4和硅酸钠,反应方程式为:Na2B4O7•lOH2O+16Na+8H2+7SiO2=4NaBH4+7Na2SiO3;
故答案为:4H3BO3+2NaOH+3H2O=Na2B4O7•lOH2O;Na2B4O7•lOH2O+16Na+8H2+7SiO2=4NaBH4+7Na2SiO3.
点评 本题考查物质制备工艺流程,为高考常见题型,涉及物质的分离与提纯、对原理与条件控制分析、盐类水解等,关键是对工艺流程理解,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案| A. | 蛋白质属于天然有机高分子化合物,没有蛋白质就没有生命 | |
| B. | HCHO溶液或(NH4)2SO4溶液均能使蛋白质变性 | |
| C. | 某些蛋白质跟浓硝酸作用会变黄 | |
| D. | 可以采用多次盐析或多次渗析的方法分离、提纯蛋白质 |
| A. | 3NO2+H2O═2HNO3+NO | B. | 4FeS2+11O2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8SO2 | ||
| C. | 3Cl2+8NH3═N2+6NH4Cl | D. | 2Na+2NH3(液)═2NaNH2+H2↑ |
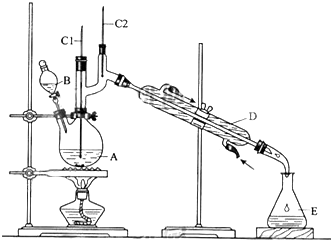
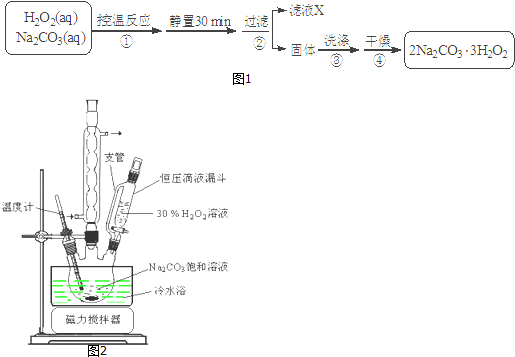
发生的反应过程如下:
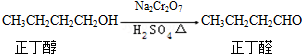
反应物和产物的相关数据如下:
| 沸点/℃ | 密度(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.5 | 0.8107 | 微溶 |
①将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.
②在A中加入5.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分.
③将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g.
回答下列问题:
(1)B仪器的名称是滴液漏斗,D仪器的名称是直形冷凝管.
(2)沸石的作用是防止暴沸.
(3)将正丁醛粗产品置于分液漏斗中分液时,水在下层(填“上”或“下”)
(4)反应温度应保持在90~95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
(5)本实验中,正丁醛的产率为51%
| A. | 凡需加热的反应是吸热反应 | B. | 只有分解反应才是吸热反应 | ||
| C. | 使用催化剂的反应是吸热反应 | D. | 氧化还原反应不一定是放热反应 |
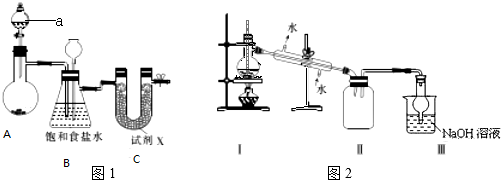
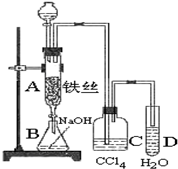 实验室用图装置制取少量溴苯,试填写下列空白.
实验室用图装置制取少量溴苯,试填写下列空白.