题目内容
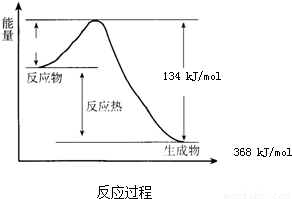
 在400℃、101kPa时,NO2(g)+CO(g)?NO(g)+CO2(g)反应过程的能量变化如图所示.
在400℃、101kPa时,NO2(g)+CO(g)?NO(g)+CO2(g)反应过程的能量变化如图所示.(1)该反应是
放热
放热
(填“吸热”或“放热”)反应.(2)该反应的热化学方程式为
NO2(g)+CO(g)?NO(g)+CO2(g)△H=-234KJ?mol-1
NO2(g)+CO(g)?NO(g)+CO2(g)△H=-234KJ?mol-1
.(3)改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的是
d
d
.a.浓度 b.压强 c.温度 d.催化剂.
分析:(1)反应物的能量高于生成物的能量时,反应是放热反应;
(2)根据热化学方程式的书写需注意标明物质的聚集状态来解答;
(3)催化剂能降低活化能.
(2)根据热化学方程式的书写需注意标明物质的聚集状态来解答;
(3)催化剂能降低活化能.
解答:解:(1)因反应物的能量高于生成物的能量时,反应是放热反应,故答案为:放热;
(2)由图知没反应放出的热量为368KJ?mol-1-134KJ?mol-1=234KJ?mol-1,且该反应为放热反应,热化学方程式为NO2(g)+CO(g)?NO(g)+CO2(g)△H=-234KJ?mol-1,
故答案为:NO2(g)+CO(g)?NO(g)+CO2(g)△H=-234KJ?mol-1;
(3)催化剂能降低活化能,加快反应速率,故答案为:d.
(2)由图知没反应放出的热量为368KJ?mol-1-134KJ?mol-1=234KJ?mol-1,且该反应为放热反应,热化学方程式为NO2(g)+CO(g)?NO(g)+CO2(g)△H=-234KJ?mol-1,
故答案为:NO2(g)+CO(g)?NO(g)+CO2(g)△H=-234KJ?mol-1;
(3)催化剂能降低活化能,加快反应速率,故答案为:d.
点评:本题考查吸热反应和放热反应、热化学方程式的数学、催化剂等,注意催化剂能降低活化能,加快反应速率.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
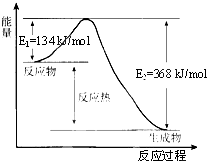 在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如图所示.下列说法不正确的是( )
在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如图所示.下列说法不正确的是( )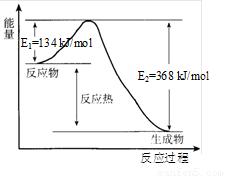
 NO2(g)+CO(g)△H
=+234 kJ/mol
NO2(g)+CO(g)△H
=+234 kJ/mol