题目内容
12.在一定条件下发生下列反应,其中属于盐类水解反应的是( )| A. | NH4++2H2O?NH3•H2O+H3O+ | B. | AlO2-+HCO3-+H2O═Al(OH)3↓+CO32- | ||
| C. | HS-+H+?H2S | D. | Cl2+H2O?H++Cl-+HClO |
分析 在盐中有弱酸根离子或弱碱离子时,与水电离产生的氢离子或氢氧根离子结合生成弱电解质,则发生的反应为盐类的水解反应,以此来解答.
解答 解:A.铵根离子为弱碱离子,结合水电离产生的OH-,水解反应为NH4++2H2O?NH3•H2O+H3O+,故A正确;
B.碳酸氢根离子水解生成碳酸,而HCO3-+H2O?H3O++CO32-为电离反应,则AlO2-+HCO3-+H2O═Al(OH)3↓+CO32-为复分解反应,故B错误;
C.HS-+H+═H2S中没有水参加反应,则不属于水解反应,HS-水解生成H2S和OH-,故C错误;
D.氯气为单质,Cl2+H2O?H++Cl-+HClO不属于水解反应,故D错误;
故选A.
点评 本题考查盐类水解的原理及离子反应,为高频考点,明确盐中的构成及“有弱才水解的规律”即可解答,注意离子结合水电离产生的氢离子或氢氧根离子结合生成弱电解质是解答的关键,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
2.下列化合物,按其晶体的熔点由高到低排列正确的是( )
| A. | SiO2 CsCl CBr4 CF4 | B. | SiO2 CsCl CF4 CBr4 | ||
| C. | CsCl SiO2 CBr4 CF4 | D. | CF4CBr4CsCl SiO2 |
3.下列各项中前后两个叙述都正确的是( )
| A. | 单质分子中一定存在共价键;最外层有2个电子的原子都是金属原子 | |
| B. | 非极性键可以存在于离子化合物中; 质子数相同的粒子不一定属于同种元素 | |
| C. | 同位素的化学性质几乎完全相同;任何原子的原子核都是由质子和中子构成的 | |
| D. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构; 伴有能量变化的物质变化都是化学变化 |
20.下列说法正确的是( )
| A. | 对于相同pH的弱酸HX和HY(前者的Ka较小),加水稀释后pH值仍相同,则前者酸中稀释的倍数更大 | |
| B. | 在CH3COOH和CH3COONa浓度均为0.1mol/L的体系中,外加少量强碱时,溶液的PH值发生较大变化 | |
| C. | 在Na2HPO4水溶液中存在关系式:c(H3PO4)+c(H2PO4-)+c(HPO42-)+c(PO43-)═c(Na+) | |
| D. | 沉淀溶解平衡BaSO4═Ba2++SO42- 的沉淀溶解平衡常数为1.1×10-10,说明难溶盐BaSO4是弱电解质 |
7.用铁片与稀硫酸反应制取氢气时,下列措施能使氢气生成速率加大的是( )
| A. | 加少量CH3COONa固体 | B. | 加水 | ||
| C. | 不用稀硫酸,改用98%浓硫酸 | D. | 用含有杂质铜的铁片 |
17.下列叙述正确的是( )
| A. | 浓度均为0.1 mol•L-1的CH3COOH和CH3COONa溶液等体积混合所得的溶液中:c(CH3COOH)+c(CH3COO-)═0.2 mol•L-1 | |
| B. | 0.1 mol•L-1 NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) | |
| C. | 0.2 mol•L-1 HCl溶液与等体积0.1 mol•L-1 NaOH溶液混合后,溶液的pH=1 | |
| D. | 0.1 mol•L-1氨水中滴入0.1 mol•L-1盐酸至溶液呈中性时:c(NH4+)=c(Cl-) |
4.下列说法不正确的是( )
| A. | 金属的冶炼原理,就是运用氧化还原反应原理,在一定条件下将金属从其化合物中还原出来 | |
| B. | 有些活泼金属如铝可作热还原法的还原剂 | |
| C. | 用电解熔融NaCl的方法来冶炼金属钠 | |
| D. | 用焦炭或一氧化碳还原氧化铝的方法来冶炼铝 |
1. 现使用酸碱中和滴定法测定市售白醋的浓度.
现使用酸碱中和滴定法测定市售白醋的浓度.
Ⅰ.实验步骤:
(1)取10.00mL市售白醋放入烧杯(填仪器名称,下同)中,用水稀释后转移到100mL容量瓶中,洗涤、转移、定容、摇匀即得待测白醋溶液.
(2)取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴酚酞作指示剂.
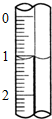
(3)读取盛装0.1000mol/L NaOH 溶液的滴定管的初始读数.如果液面位置如右图所示,则此时的读数为1.10mL.
(4)滴定时一手控制活塞,一手握住锥形瓶颈轻轻摇动,双眼注视锥形瓶中溶液的颜色变化.当溶液由无色恰好变为浅红色,并在半分钟内不褪色时,
停止滴定,并记录NaOH溶液的终读数.重复滴定3次.
Ⅱ.实验记录:
Ⅲ.数据处理与讨论:
(5)甲同学在处理数据时计算得:
平均消耗的NaOH溶液的体积V=$\frac{(14.95+16.05+15.95)}{3}$=15.65(mL)
乙同学认为处理数据时第一次实验的数据应该舍去,原因是第1次数据误差明显过大,属异常值,应舍去.
按正确数据处理,可得c(市售白醋)=0.80mol/L.
(6)在本实验的滴定过程中,下列操作会使实验结果偏大的是ab(填写序号).
a.滴定管在滴定时未用标准NaOH溶液润洗
b.滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出.
 现使用酸碱中和滴定法测定市售白醋的浓度.
现使用酸碱中和滴定法测定市售白醋的浓度.Ⅰ.实验步骤:
(1)取10.00mL市售白醋放入烧杯(填仪器名称,下同)中,用水稀释后转移到100mL容量瓶中,洗涤、转移、定容、摇匀即得待测白醋溶液.
(2)取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴酚酞作指示剂.
(3)读取盛装0.1000mol/L NaOH 溶液的滴定管的初始读数.如果液面位置如右图所示,则此时的读数为1.10mL.
(4)滴定时一手控制活塞,一手握住锥形瓶颈轻轻摇动,双眼注视锥形瓶中溶液的颜色变化.当溶液由无色恰好变为浅红色,并在半分钟内不褪色时,
停止滴定,并记录NaOH溶液的终读数.重复滴定3次.
Ⅱ.实验记录:
次数 数据(mL) | 1 | 2 | 3 |
| V(样品) | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 14.95 | 16.05 | 15.95 |
(5)甲同学在处理数据时计算得:
平均消耗的NaOH溶液的体积V=$\frac{(14.95+16.05+15.95)}{3}$=15.65(mL)
乙同学认为处理数据时第一次实验的数据应该舍去,原因是第1次数据误差明显过大,属异常值,应舍去.
按正确数据处理,可得c(市售白醋)=0.80mol/L.
(6)在本实验的滴定过程中,下列操作会使实验结果偏大的是ab(填写序号).
a.滴定管在滴定时未用标准NaOH溶液润洗
b.滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出.
2.下列关于有机物的说法中,不正确的是( )
| A. | 液化石油气和天然气的主要成分都是甲院 | |
| B. | 苯、乙醇和乙酸都能发生取代反应 | |
| C. | 油脂在碱的催化作用下可发生水解,工业上利用该反应生产肥皂 | |
| D. | 煤的气化是化学变化,石油分馏是物理变化 |