题目内容
下列关于实验操作能实现目的是( )
A、 分离碘酒中的碘和酒精 |
B、 实验室制氨气 |
C、 除去Cl2中的HCl |
D、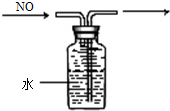 排水集气法收集NO |
考点:化学实验方案的评价
专题:实验评价题
分析:A.碘与酒精不分层;
B.氯化铵分解后在管口又化合生成氯化铵;
C.二者均与NaOH反应;
D.NO不溶于水,导管短进长出.
B.氯化铵分解后在管口又化合生成氯化铵;
C.二者均与NaOH反应;
D.NO不溶于水,导管短进长出.
解答:
解:A.碘与酒精不分层,不能分液分离,应蒸馏,故A错误;
B.氯化铵分解后在管口又化合生成氯化铵,则不能用于制取氨气,应选氯化铵与碱石灰共热,故B错误;
C.二者均与NaOH反应,应选饱和食盐水,故C错误;
D.NO不溶于水,导管短进长出,且集气瓶中装满水,装置合理,故D正确;
故选D.
B.氯化铵分解后在管口又化合生成氯化铵,则不能用于制取氨气,应选氯化铵与碱石灰共热,故B错误;
C.二者均与NaOH反应,应选饱和食盐水,故C错误;
D.NO不溶于水,导管短进长出,且集气瓶中装满水,装置合理,故D正确;
故选D.
点评:本题考查化学实验方案的评价,涉及混合物的分离、提纯、气体的制备及收集、除杂等,侧重实验装置及分离原理的考查,注重实验的评价性和可行性分析,题目难度不大.

练习册系列答案
相关题目
NA为阿伏加德罗常数,下列说法中正确的是( )
| A、22.4 L Cl2中含有NA个Cl2分子 |
| B、标准状况下,22.4L CCl4中含有的CCl4分子数为NA |
| C、1.0 L 浓度为18mol?L-1H2SO4溶液与足量的铜片加热条件下反应,被还原的H2SO4的分子数为9NA |
| D、一定条件下,2.3gNa完全与O2反应生成3.6g产物时失去的电子数为0.1NA |
某能使酚酞变红的无色透明的溶液中能大量共存离子组是( )
| A、Fe3+ K+ SO42- NO3- |
| B、Mg2+ NH4+ SO42- Cl- |
| C、Na+ K+ SO42- NO3- |
| D、K+ Na+ MnO4- SO42- |
下列说法正确的是( )
| A、原电池的负极是电子流出的一极,电极上发生氧化反应 |
| B、原电池反应一定是释放能量的置换反应 |
| C、电解可以使通常条件下不能发生的氧化还原反应得以发生 |
| D、电解池中,连接电源正极的一极叫阳极,发生还原反应 |
节能减排成为社会发展过程中不可回避的问题.下列说法正确的是( )
①推广乙醇汽油可以减轻环境污染,降低尾气中一氧化碳含量.
②乙醇汽油作为一种新型清洁燃料,是目前世界上可再生能源的发展重点之一.
③乙醇属于可再生资源,使用乙醇汽油可以缓解目前石油紧缺的矛盾.
④太阳能、风能、水能、生物质能、地热能和海洋能等都属于可再生能源.
⑤乙醇属于一级能源.
①推广乙醇汽油可以减轻环境污染,降低尾气中一氧化碳含量.
②乙醇汽油作为一种新型清洁燃料,是目前世界上可再生能源的发展重点之一.
③乙醇属于可再生资源,使用乙醇汽油可以缓解目前石油紧缺的矛盾.
④太阳能、风能、水能、生物质能、地热能和海洋能等都属于可再生能源.
⑤乙醇属于一级能源.
| A、①②⑤ | B、①②③ |
| C、③④ | D、①②③④ |
碱性锌锰电池是一种常见的一次电池,应用非常广泛,其工作时发生如下反应:Zn+2MnO2+H2O=2MnOOH+Zn(OH)2,则( )
| A、Zn为负极,MnO2为正极 |
| B、MnO2为正极,Zn为负极 |
| C、工作时电子由MnO2经外电路流向Zn极 |
| D、Zn电极发生还原反应,MnO2电极发生氧化反应 |

 有位于周期表前四周期的A、B、C、D、E、F六种元素,其原子序数依次增大.已知A原子核外有三个未成对电子;A与B形成的一种化合物常温下是红棕色气体;化合物C2E的晶体为离子晶体;D单质的熔点在同周期单质中最高;E原子核外的M层中只有两对成对电子;F原子核外最外层电子数与C相同,其余各层均充满.请根据以上信息,回答下列问题:
有位于周期表前四周期的A、B、C、D、E、F六种元素,其原子序数依次增大.已知A原子核外有三个未成对电子;A与B形成的一种化合物常温下是红棕色气体;化合物C2E的晶体为离子晶体;D单质的熔点在同周期单质中最高;E原子核外的M层中只有两对成对电子;F原子核外最外层电子数与C相同,其余各层均充满.请根据以上信息,回答下列问题: