题目内容
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.1mol甲醇中含有C—H键的数目为4NA |
| B.25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C.Na2O2与足量H2O反应产生0.2mol O2,转移电子的数目为0.4NA |
| D.标准状况下,2.24 L己烷含有分子的数目为0.1 NA |
C
解析试题分析:A、1mol甲醇中含有C—H键的数目是3NA,错误;B、缺少溶液体积,无法计算OH-的数目,错误;C、Na2O2与H2O反应,每生成1mol氧气转移2mol电子,所以产生0.2mol O2,转移电子的数目为0.4NA,正确;D、.标准状况下,己烷为液态,无法计算其物质的量,错误,答案选C。
考点:考查阿伏伽德罗常数的应用

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
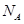 代表阿伏加德罗常数,下列说法不正确的是
代表阿伏加德罗常数,下列说法不正确的是
A.标准状况下,11.2L氯仿(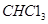 )中含有 )中含有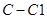 键的数目为1.5 键的数目为1.5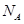 |
B.常温常压下,17g甲基(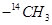 )所含的电子数为9 )所含的电子数为9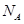 |
| C.同温同压下,1LNO和1LO2充分混合体积小于1.5L |
D.pH=l的醋酸溶液100mL中氢离子数为0.01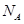 |
用NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A.在标准状况下22.4L H2中含有氢分子的个数为2NA |
| B.24g Mg变为Mg2+时失去的电子数为2NA |
| C.32g O2中含有氧原子的个数为2NA |
| D.1L 1mol/L NaCl溶液中含有钠离子的个数为NA |
在硫酸铝、硫酸钾和明矾[KAl(SO4)2·12H2O]混合溶液中,SO42—浓度为0.4mol/L,当加入等体积0.4mol/L KOH溶液时,生成的沉淀恰好完全溶解。则反应后溶液中K+的浓度约为( )
| A.0.225mol/L | B.0.25mol/L | C.0.45mol/L | D.0.9mol/L |
分析下表中三种气体物质的有关数据,下列说法不正确的是
| 物质 | 质量/g | 体 积 | ||
| 0℃,101kPa | 20℃,101kPa | 0℃,202kPa | ||
| H2 | 2 | 22.4 | 24.0 | 11.2 |
| O2 | 32 | 22.4 | 24.0 | 11.2 |
| CO2 | 44 | 22.3 | 23.9 | 11.2 |
A.物质的量相同的三种气体,在相同的条件下,其体积基本相同
B.相同的条件下,体积相同的三种气体,其质量不同
C.质量相同的三种气体,在相同的条件下,其体积一定不同
D.相同的条件下,体积相同的三种气体,因其质量不同,所以气体分子数目也不同
室温时,在体枳相同的容器内混合下列气体。混合后压强最小的是 ( )
| A.100mL H2和50mL O2 | B.100mL N2和200mL O2 |
| C.100mL NO和100mL O2 | D.100mL HCl和100mL NH3 |
在一定的温度和压强下,1体积X2(气)跟3体积Y2(气)化合生成2体积化合物(气),则该化合物的化学式是( )。
| A.XY3 | B.XY | C.X3Y | D.X2Y3 |
氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是
| A.H2O2分子中只存在极性键 |
B.NH3的结构式为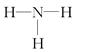 |
C.HCl的电子式为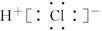 |
D.H2O的比例模型为 |