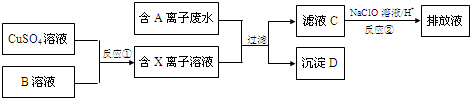
题目内容
4.15g某气体化合物甲在标准状况下的体积为11.2L,则甲的相对分子质量为30.分析 根据n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$计算.
解答 解:n=$\frac{11.2L}{22.4L/mol}$=0.5mol,M=$\frac{15g}{0.5mol}$=30g/mol,
故答案为:30.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析能力的考查,注意把握相关公式的运用,难度不大.

练习册系列答案
相关题目
14.下列关于金属铬的叙述中不正确的是( )
| A. | 铬元素在周期表中处于第四周期V IB族 | |
| B. | 铬原子的外围电子层排布为3d44s2 | |
| C. | 铬原子中,质子数为24 | |
| D. | 铬元素位于元素周期表的d区,是过渡元素 |
15.下列化学用语正确的是( )
| A. | 中子数为20的氯原子:${\;}_{17}^{37}$Cl | |
| B. | 次氯酸的电离方程式:HClO=H++ClO- | |
| C. | Na+的结构示意图: | |
| D. | 赤铁矿的主要成分:Fe3O4 |
12.向含有FeCl3、BaCl2的酸性溶液中通入足量的SO2,有白色沉淀生成,过滤,向滤液中滴入KSCN溶液时无明显现象,由此得出的正确结论是( )
| A. | 白色沉淀是BaSO3 | B. | 白色沉淀是BaSO4 | ||
| C. | 白色沉淀是BaSO3、BaSO4的混合物 | D. | FeCl3全部被SO2氧化为FeCl2 |
19.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)=CO2(g)+2H2(g);△H=-192.9kJ•mol-1
下列说法正确的是( )
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)=CO2(g)+2H2(g);△H=-192.9kJ•mol-1
下列说法正确的是( )
| A. | CH3OH的标准燃烧热为△H=-192.9 kJ•mol-1 | |
| B. | 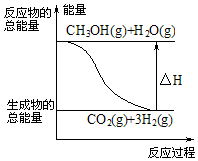 反应①中的能量变化如图所示 | |
| C. | CH3OH转变成H2的过程一定要吸收能量 | |
| D. | 根据②推知反应:CH3OH(l)+$\frac{1}{2}$O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ•mol-1 |
9.下列有机物分子中所有的原子不可能处于同一平面的是( )
| A. | 1,3-丁二烯 | B. | 乙烷 | C. | 苯乙烯 | D. | 甲醛 |
19.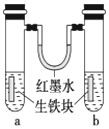 如图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和稀醋酸,各加入生铁块,放置一段时间.下列有关描述错误的是( )
如图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和稀醋酸,各加入生铁块,放置一段时间.下列有关描述错误的是( )
 如图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和稀醋酸,各加入生铁块,放置一段时间.下列有关描述错误的是( )
如图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和稀醋酸,各加入生铁块,放置一段时间.下列有关描述错误的是( )| A. | 生铁块中的碳是原电池的正极 | |
| B. | 两试管中相同的电极反应式是:Fe-2e-=Fe2+ | |
| C. | a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀 | |
| D. | 红墨水柱两边的液面变为左低右高 |