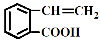题目内容
已知25℃、101kPa条件下:
4Al (s) + 3O2 (g)=2Al2O3 (s) △H=-2834.9 kJ/mol
4Al (s) + 2O3 (g) = 2Al2O3 (s) △H= -3119.91kJ/mol
由此得出的结论正确的是
A.等质量的O2比O3能量低,由O2变O3 为放热反应
B.等质量的O2比O3能量低,由O2变O3 为吸热反应
C.3O2(g)=2O3 (g) △H=285.0 kJ/mol
D.O3比O2稳定,由O2变O3 为吸热反应
BC
【解析】
试题分析:4Al (s)+3O2(g)═2Al2O3 (s)△H=-2834.9kJ?mol-1 ①
4Al (s)+2O3 (g)═2Al2O3 (s)△H=-3119.91kJ?mol-1 ②
①-②得3O2(g)═2O3 △H=+285.01kJ?mol-1 该反应吸热,等质量的O2比O3能量低,所以O2比O3稳定,由O2变O3为吸热反应,故选:BC。
考点:考查盖斯定律以及能量与稳定性的关系

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
 O2(g)═CO(g)△H1=-110.5kJ/mol
O2(g)═CO(g)△H1=-110.5kJ/mol cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
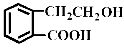 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质: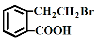 ②
② ③
③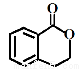 ④
④