题目内容
4.已知3mol碳在2mol氧气中燃烧,至反应物耗尽,测得放出热量akJ,又知0.1mol碳完全燃烧,放出热量为bkJ.则化学方程式C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=Q中Q等于( )| A. | -(a-b)kJ•mol-1 | B. | -(a+b)kJ•mol-1 | ||
| C. | -(5a-0.5b)kJ•mol-1 | D. | -(0.5a-5b)kJ•mol-1 |
分析 碳在氧气中燃烧,氧气不足发生反应2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO,氧气足量发生反应C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;3mol碳在2mol氧气中燃烧,n(C):n(O2)=3:2,介于2:1与1:1之间,所以上述反应都发生.令生成的CO为xmol,CO2为ymol,根据碳元素与氧元素守恒列方程计算x、y的值,计算生成ymol二氧化碳方程的热量,放出的总热量减去生成二氧化碳放出的热量为生成xmolCO放出的热量,据此计算1molC与O2反应生成CO的反应热△H.
解答 解:碳在氧气中燃烧,氧气不足发生反应2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO,氧气足量发生反应C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;
3mol碳在2mol氧气中燃烧,n(C):n(O2)=3:2,介于2:1与1:1之间,
设生成的CO为xmol,CO2为ymol,
根据碳元素守恒有x+y=3,根据氧元素守恒有x+2y=2×2,联立方程解得:x=2,y=1,
0.1mol碳完全燃烧,放出热量为 b kJ,则1mol碳完全燃烧,放出热量为10b kJ,
所以生成1molCO放出的热量为0.5×(akJ-10bkJ).
由于碳燃烧为放热反应,所以反应热△H的符号为“-”,
故1mol C与O2反应生成CO的反应热△H=-0.5×(akJ-10bkJ)=-(0.5a-5b) kJ•mol-1,
故选D.
点评 本题考查反应热的计算,题目难度不大,判断碳与氧气反应产物中一氧化碳与二氧化碳的物质的量是关键,注意反应热△H的单位与符号,试题培养了学生的化学计算能力.

 全优点练单元计划系列答案
全优点练单元计划系列答案| A. | 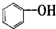 属于醇类化合物 属于醇类化合物 | B. | 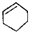 属于芳香族化合物 属于芳香族化合物 | ||
| C. | 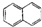 属于脂环化合物 属于脂环化合物 | D. | CH3CH(CH3)2属于链状化合物 |
| A. | 辛烯和3-甲基-1-丁烯 | B. | 甲苯和乙炔 | ||
| C. | 1-氯丙烷和2-氯丙烷 | D. | 甲基环己烷和己烯 |
| A. | 人类利用能源的三个阶段分别是:柴草时期、化石能源时期、多能源结构时期 | |
| B. | 人类使用沼气是对化学能的充分利用 | |
| C. | 发展低碳经济、循环经济,开发推广太阳能、水能、风能等能源,减少煤、石油等化石燃料的使用 | |
| D. | 生物质能主要指用树木、庄稼、草类等植物直接或间接提供的能量,它是不可再生的能源 |

 (不考虑空间构型,如有配位键,请标出)
(不考虑空间构型,如有配位键,请标出)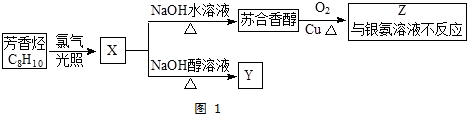
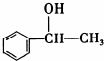 ,它不能发生的有机反应类型有④、⑥.
,它不能发生的有机反应类型有④、⑥.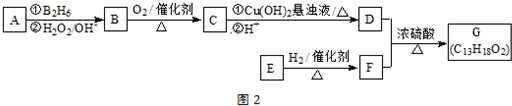
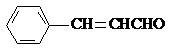 .
.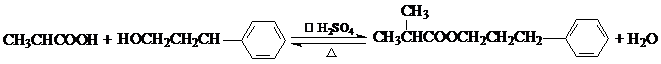 .
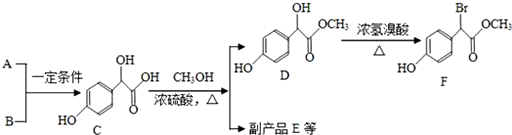
.
 .
.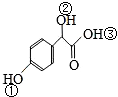 中①、②、③3个-OH的酸性有强到弱的顺序是:③>①>②.
中①、②、③3个-OH的酸性有强到弱的顺序是:③>①>②.