题目内容
电解质溶液有许多奇妙之处,你只有深入思考,才能体会到它的乐趣.下列关于电解质溶液的叙述中正确的是( )
| A、Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 |
| B、常温下,1 mol?L-1的CH3COOH溶液与1 mol?L-1的NaOH溶液等体积混合后,所得混合液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C、将AlCl3溶液加热蒸干并灼烧后剩余固体为Al2O3 |
| D、常温下,某溶液中由水电离出的c(H+)=10-5 mol?L-1,则此溶液可能是盐酸 |
考点:离子浓度大小的比较,水的电离,盐类水解的原理
专题:盐类的水解专题
分析:A.Na2CO3、NaHCO3两种盐溶液中阳离子都是Na+、H+,阴离子CO32-、HCO3-、OH-;
B.阳离子浓度大于阴离子浓度,电荷不守恒;
C.水解氢氧化铝和盐酸,盐酸易挥发,加热是氢氧化铝分解;
D.常温下,某溶液中由水电离出的c(H+)=10-5 mol?L-1,水的电离增大,平衡正向移动,应为盐溶液.
B.阳离子浓度大于阴离子浓度,电荷不守恒;
C.水解氢氧化铝和盐酸,盐酸易挥发,加热是氢氧化铝分解;
D.常温下,某溶液中由水电离出的c(H+)=10-5 mol?L-1,水的电离增大,平衡正向移动,应为盐溶液.
解答:
解:A.Na2CO3、NaHCO3两种盐溶液中阳离子都是Na+、H+,阴离子CO32-、HCO3-、OH-,离子种类相同,故A错误;
B.选项中离子浓度大小不符合溶液电中性原则,应为c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故B错误;
C.水解氢氧化铝和盐酸,盐酸易挥发,加热是氢氧化铝分解,最后剩余固体为Al2O3,故C正确.
D.常温下,水的离子积为10-14,水电离出的c(H+)=c(OH-)=10-7,酸或碱的溶液抑制水的电离,该溶液中c(H+)=10-5mol?L-1,水的电离程度增大,则此溶液不可能是盐酸,可能是强酸弱碱盐,故D错误.
故选:C.
B.选项中离子浓度大小不符合溶液电中性原则,应为c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故B错误;
C.水解氢氧化铝和盐酸,盐酸易挥发,加热是氢氧化铝分解,最后剩余固体为Al2O3,故C正确.
D.常温下,水的离子积为10-14,水电离出的c(H+)=c(OH-)=10-7,酸或碱的溶液抑制水的电离,该溶液中c(H+)=10-5mol?L-1,水的电离程度增大,则此溶液不可能是盐酸,可能是强酸弱碱盐,故D错误.
故选:C.
点评:本题考查溶液中离子浓度的大小比较,为高频考点,难度中等,离子浓度比较,注意考虑电离、水解、水的电离、微粒守恒、电荷守恒、质子恒等式等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质的使用不涉及化学变化的是( )
| A、过氧化钠作供氧剂 |
| B、液氨用作致冷剂 |
| C、福尔马林作防腐剂 |
| D、生石灰作干燥剂 |
下列操作错误的是( )
| A、Cu中混有CuO,可以通过加入足量盐酸溶液,再过滤、洗涤、干燥可得到洁净的Cu |
| B、把1 mL饱和FeCl3溶液逐滴加入到20 mL的沸水中,边加边搅拌,加热到沸腾即可得Fe(OH)3胶体 |
| C、蒸发结晶时当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干 |
| D、进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
咖啡酸可用作化学原料的中间体,其结构如图.下列关于咖啡酸的说法中正确的是( )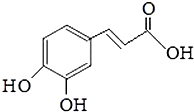

| A、分子中所有官能团均能与NaOH反应,且反应原因相同 |
| B、一定条件下,咖啡酸能够发生取代反应、加聚反应、缩聚反应,但不能与NaHCO3溶液反应 |
| C、分子中的所有碳原子可能共平面,但氧原子不可能与所有碳原子处于同一平面上 |
| D、咖啡酸与浓溴水反应,一个咖啡酸分子中最多能引入5个溴原子 |
下列溶液中微粒的物质的量浓度关系一定正确的是( )
| A、0.1 mol?L-1的NH4Cl溶液与0.05 mol?L-1的NaOH溶液等体积混合后显碱性的溶液:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) |
| B、等物质的量的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C、pH=2的HA溶液与pH=12的MOH溶液等体积混合:c(M+)=c(A-)>c(OH-)=c(H+) |
| D、某二元弱酸的酸式盐NaHA溶液:c(OH-)+c(H2A)=c(H+)+2c(A2-) |
常温下,将0.2mol/L NaA溶液和0.1mol/L盐酸等体积混合后,溶液pH>7,以下关系式错误的是( )
| A、电荷守恒:c(Na+)+c(H+)=c(A-)+c(Cl-)+c(OH-) |
| B、物料守恒:c(HA)+c(A-)=0.1mol/L |
| C、质子守恒:c(HA)+c(H+)=c(A-)+c(OH-) |
| D、物料守恒:c(Na+)=c(A-)+c(HA) |