题目内容
2.有下列5种物质:①Ar、②CO2、③KOH、④K2S、⑤Na2O2.微粒中只存在共价键的是②;只存在离子键的是④;既存在离子键,又存在极性共价键的是③;既存在离子键,又存在非极性共价键的是⑤;不存在化学键的是①.(用编号填空)分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,同种非金属元素形成非极性共价键,不同种非金属元素形成极性共价键,以此来解答.
解答 解:①Ar不含化学键;
②CO2中只含C、O之间的极性共价键;
③KOH中含离子键和O-H极性共价键;
④K2S中只含离子键;
⑤Na2O2中离子键和O-O非极性键;
则只存在共价键的是②,只存在离子键的是④,既存在离子键又存在极性共价键的是③,既存在离子键又存在非极性共价键的是⑤;不存在化学键的是①.
故答案为:②;④;③;⑤;①.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.

练习册系列答案
相关题目
11.如图是一些常见的有机物的转化关系.下列说法错误的是( )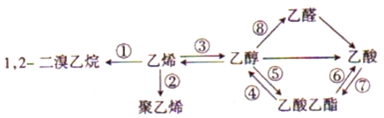

| A. | 反应①、③均属于加成反应 | B. | 乙酸与甲酸甲酯互为同分异构体 | ||
| C. | 乙醇溶液可除去暖瓶中的水垢 | D. | 反应④、⑤、⑥、⑦均属于取代反应 |
12.对于反应Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g),下列叙述不正确的是( )
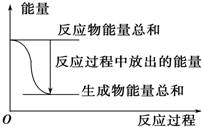

| A. | 其反应物或生成物都能用来表示该反应的速率 | |
| B. | 反应过程中能量关系可用如图表示 | |
| C. | 若将该反应设计成原电池,锌为负极 | |
| D. | 若设计为原电池,当有32.5g锌溶解,标准状况下正极放出11.2L气体 |
17.下列由相关实验现象所推出的结论正确的是( )
| A. | 向某溶液中加入适量的 AgNO3溶液,有白色沉淀产生,则原溶液中一定有 Cl- | |
| B. | 向某溶液中加入稀盐酸无明显现象,再加 AgNO3溶液有白色沉淀产生,则原溶液中一定有Cl- | |
| C. | 向某溶液中加入 BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不溶解,则原溶液中一定有SO42- | |
| D. | 向某溶液中加入稀盐酸,无明显现象,再加 BaCl2溶液有白色沉淀产生,则原溶液中一定有SO42- |
7.298K时,向50mL溶有0.1molCl2的氯水中滴加2mol•L-1的NaOH溶液,溶液pH随所加NaOH溶液体积变化的图象如下.下列说法正确的是( )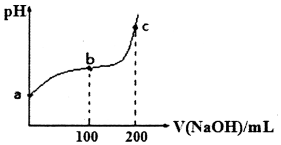

| A. | b~c段,随着NaOH溶液的滴入,$\frac{c(HClO)}{c(Cl{O}^{-})}$逐渐增大 | |
| B. | 若a点pH=4,且c(Cl-)=100c(ClO-),则Ka(HClO)=$\frac{1{0}^{-4}}{101}$ | |
| C. | b点对应的溶液可用pH试纸测定其pH | |
| D. | c点对应的溶液中:c(Na+)>c(OH-)>c(C1-)>c(C1O-)>c(H+) |
11.下列叙述Ⅰ和Ⅱ均正确并用因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 纳米铁粉有很好的吸附性 | 纳米铁粉可以高效地去除被污染水体中 的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子 |
| B | 硅胶可以和水发生化学反应 | 硅胶作袋装食品的干燥剂 |
| C | SO3有毒 | 不能做食品防腐剂 |
| D | 肥皂水显碱性 | 肥皂水作蚊虫叮咬处的清洗剂 |
| A. | A | B. | B | C. | C | D. | D |
12.X、Y、Z、W是原子序数依次增大的四种短周期元素,p、q、r、s是上述四种元素形成的二元化合物,其中r是一种中学常见的两性氧化物,s是一种强酸,r与s的水溶液反应生成P与q.下列说法错误的是( )
| A. | 简单离子半径:W>Y>Z | B. | 气态氢化物的沸点:Y>W | ||
| C. | Y与W可以形成多种二元化合物 | D. | p、q与r的化学键类型完全相同 |
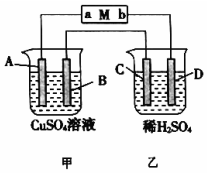 如图所示装置中,当线路接通时,发现M 滤纸(用Na2SO4溶液的石蕊试液浸润过)的a端显蓝色,b端显红色,且知甲中电极材料是锌、银,乙中电极材料是铂、铜,且乙中两电极不发生变化.回答:
如图所示装置中,当线路接通时,发现M 滤纸(用Na2SO4溶液的石蕊试液浸润过)的a端显蓝色,b端显红色,且知甲中电极材料是锌、银,乙中电极材料是铂、铜,且乙中两电极不发生变化.回答: