题目内容
5.部分短周期元素的性质或原子结构如表所示.| 元素代号 | 元素的性质或原子结构 |
| W | M层上的电子数为4 |
| X | 常温下,其单质为双原子分子,其氢化物的水溶液显碱性 |
| Y | L层电子数为次外层电子数的3倍 |
| Z | 元素最高正价是+7价 |
| A. | 原子半径:W>X>Y | |
| B. | 化合物WY2不溶于水 | |
| C. | 由X、Y和氢三种元素形成的所有化合物中只含共价键 | |
| D. | 最高价氧化物对应水化物的酸性:W<Z |
分析 W的M层上的电子数为4,为Si元素,X常温下,其单质为双原子分子,其氢化物的水溶液显碱性,为N元素,Y的L层电子数为次外层电子数的3倍,为O元素,Z的元素最高正价是+7价,为Cl元素,结合对应单质、化合物的性质以及元素周期率知识解答该题.
解答 解:由以上分析可知W为Si元素、X为N元素、Y为O元素、Z为Cl元素.
A.同主族元素的单质从上到下,原子半径逐渐增大,同周期元素的单质从左到右,原子半径逐渐减小,则W>X>Y,故A正确;
B.二氧化硅不溶于水,故B正确;
C.由X、Y和氢三种元素形成的所有化合物如为硝酸铵,则为离子化合物,含共价键和离子键,故C错误;
D.非金属性Si<Cl,元素的非金属性越强,对应的最高价氧化物对应水化物的酸性越强,故D正确.
故选C.
点评 本题主要考查了元素周期律以及原子核外电子排布知识,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意把握原子的结构特点.

练习册系列答案
相关题目
15.为了提纯下列物质(括号内为杂质),所选除杂试剂,分离方法,必用仪器都正确的是( )
| 选项 | 不纯物质 | 除杂试剂 | 分离方法 | 必用仪器 |
| A | 碘(水) | 四氯化碳 | 萃取 | 分液漏斗 |
| B | 氯化钾(氯化钙) | 适量盐酸 | 过滤 | 玻璃棒 |
| C | 硝酸铜(硝酸银) | 适量铜粉 | 结晶 | 酒精灯 |
| D | 硫酸钾(碳酸钾) | 适量盐酸 | 蒸馏 | 温度计 |
| A. | A | B. | B | C. | C | D. | D |
13.氯酸钾是常见的氧化剂,用于制造火药、烟火,工业上用石灰乳氯化法制备氯酸钾的流程如图所示:
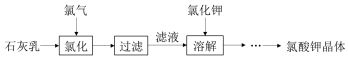
已知:氯化过程主要发生反应 6Ca(OH)2+6Cl2$\stackrel{△}{→}$5CaCl2+Ca(ClO3)2+6H2O
完成下列填空:
(1)工业生产氯气的方法是电解饱和食盐水.
(2)氯化过程需要控制较高温度,其目的有:
①加快反应速率; ②减少 Cl2与 Ca(OH)2之间的副反应.
(3)向热的滤液中加入稍过量的氯化钾,待溶解完全后进行冷却,有大量氯酸钾晶体析出,写出相关反应
的化学方程式:Ca(ClO3)2+2KCl=CaCl2+2KClO3↓.
得到的氯酸钾晶体中可能会含有少量氯化钾,进一步提纯的方法是重结晶.
(4)为测定所得晶体中氯酸钾的纯度,将 a g 样品与 b g 二氧化锰混合,加热该混合物一段时间后(杂质
不参加反应)冷却,称量剩余固体质量,重复加热、冷却、称量操作,记录数据如表:
①进行加热操作时,应将固体置于坩埚(填仪器名称)中.
②该实验不必进行第五次加热的原因是剩余固体质量已恒重,说明KClO3已分解完全.
③若某次测定结果的相对误差为-2.98%,写出导致这一结果的一种可能情况.未在干燥器中冷却,剩余固体吸水(加热时间不足,氯酸钾未完全分解).

已知:氯化过程主要发生反应 6Ca(OH)2+6Cl2$\stackrel{△}{→}$5CaCl2+Ca(ClO3)2+6H2O
完成下列填空:
(1)工业生产氯气的方法是电解饱和食盐水.
(2)氯化过程需要控制较高温度,其目的有:
①加快反应速率; ②减少 Cl2与 Ca(OH)2之间的副反应.
(3)向热的滤液中加入稍过量的氯化钾,待溶解完全后进行冷却,有大量氯酸钾晶体析出,写出相关反应
的化学方程式:Ca(ClO3)2+2KCl=CaCl2+2KClO3↓.
得到的氯酸钾晶体中可能会含有少量氯化钾,进一步提纯的方法是重结晶.
(4)为测定所得晶体中氯酸钾的纯度,将 a g 样品与 b g 二氧化锰混合,加热该混合物一段时间后(杂质
不参加反应)冷却,称量剩余固体质量,重复加热、冷却、称量操作,记录数据如表:
| 加热次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 剩余固体质量(g) | c | d | e | e |
②该实验不必进行第五次加热的原因是剩余固体质量已恒重,说明KClO3已分解完全.
③若某次测定结果的相对误差为-2.98%,写出导致这一结果的一种可能情况.未在干燥器中冷却,剩余固体吸水(加热时间不足,氯酸钾未完全分解).
20.下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 取等物质的量的两种金属单质X、Y,分别与足量的盐酸反应 | X产生氢气的体积比Y多 | 金属性:X>Y |
| B | 用玻璃棒蘸取浓硫酸点到蓝色石蕊试纸上 | 试纸变黑 | 浓硫酸具有脱水性 |
| C | 将蘸有浓氨水的玻璃棒置于某无机酸浓溶液的试剂瓶口 | 有大量白烟 | 该无机酸一定为盐酸 |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| A. | A | B. | B | C. | C | D. | D |
10.铁及其化合物在生产和生活中有广泛的应用.
Ⅰ、高铁酸钠(Na2FeO4)是一种新型净水剂,工业上制备高铁酸钠的反应原理为:
Fe(OH)3+NaClO+NaOH→Na2FeO4+X+H2O(未配平),则X的电子式为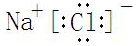 ,反应中被氧化的物质是Fe(OH)3(写化学式).
,反应中被氧化的物质是Fe(OH)3(写化学式).
Ⅱ、铁红颜料跟某些油料混合,可以制成防锈油漆.工业制硫酸产生的硫酸渣中主要含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如图:
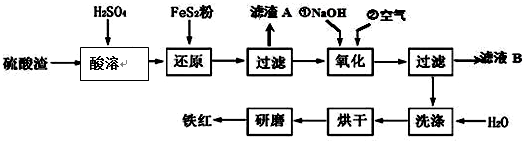
已知:
已知FeS2是一种黄色难溶于水的固体.
(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;“滤渣A”主要成份的化学式为SiO2.
(2)还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,写出该反应的离子方程式FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+.
(3)为确保铁红的质量和纯度,氧化过程中加NaOH调节溶液pH的范围是3.2~3.8;如果加NaOH调节溶液pH=a,则滤液B中c(Fe3+)=4×10(4-3a)mol/L(25℃时,Ksp=4×10-38)
(4)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可以构成燃料电池.该电池负极的电极反应式为CH3OCH3+16OH--12e-=2CO32-+11H2O.
Ⅰ、高铁酸钠(Na2FeO4)是一种新型净水剂,工业上制备高铁酸钠的反应原理为:
Fe(OH)3+NaClO+NaOH→Na2FeO4+X+H2O(未配平),则X的电子式为
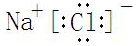 ,反应中被氧化的物质是Fe(OH)3(写化学式).
,反应中被氧化的物质是Fe(OH)3(写化学式).Ⅱ、铁红颜料跟某些油料混合,可以制成防锈油漆.工业制硫酸产生的硫酸渣中主要含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如图:

已知:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;“滤渣A”主要成份的化学式为SiO2.
(2)还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,写出该反应的离子方程式FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+.
(3)为确保铁红的质量和纯度,氧化过程中加NaOH调节溶液pH的范围是3.2~3.8;如果加NaOH调节溶液pH=a,则滤液B中c(Fe3+)=4×10(4-3a)mol/L(25℃时,Ksp=4×10-38)
(4)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可以构成燃料电池.该电池负极的电极反应式为CH3OCH3+16OH--12e-=2CO32-+11H2O.
17.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关13C、15N叙述正确的是( )
| A. | 13C与15N有相同的中子数 | B. | 13C与12C性质相同 | ||
| C. | 15N与14N互为同位素 | D. | 15N的核外电子数与中子数相同 |
14.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 22.4L氘(D2)气体,含有中子数为2NA | |
| B. | 1.6gNH2-离子所含电子数为NA | |
| C. | 4g氦气所含分子数为0.5NA | |
| D. | NA个SO3分子在标准状况下的体积为22.4L |
11.下列实验操作与预期目的或所得结论一致的是( )
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向某盐溶液中加入AgNO3溶液,产生白色沉淀;加入浓NaOH溶液加热,生成使湿润红色石蕊试纸变蓝的气体 | 该盐一定是NH4Cl |
| B | 向浓硝酸中加入足量铜片充分反应,所得气体显红棕色 | 该气体是纯净的NO2 |
| C | 常温下,向浓度均为0.01mol/L的Na2CO3和Na2SO4的混合溶液中滴加1~2滴BaCl2溶液,滤出的沉淀不溶于盐酸 | 说明常温下Ksp(BaCO3)>Ksp(BaSO4) |
| D | 向Na2O2与水反应后所得溶液中加少量MnO2 | 检验Na2O2与水反应的中 间产物为H2O2 |
| A. | A | B. | B | C. | C | D. | D |
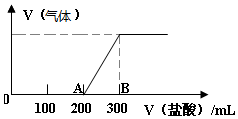 向100mL1.5mol/L的丙溶液中缓慢通入一定量的CO2,充分反应后,向所得溶液中逐滴缓慢滴加0.5mol/L的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示.
向100mL1.5mol/L的丙溶液中缓慢通入一定量的CO2,充分反应后,向所得溶液中逐滴缓慢滴加0.5mol/L的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示.