题目内容
 (1)氢是未来最好的能源选择,制取氢气的成熟的方法有很多,利用甲醇可以与水蒸气反应生成氢气,反应方程式如下:
(1)氢是未来最好的能源选择,制取氢气的成熟的方法有很多,利用甲醇可以与水蒸气反应生成氢气,反应方程式如下:CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H(298K)=+49.4kJ/mol
一定条件下,向容积为2L的恒容密闭容器中充入1mol CH3OH(g)和3mol H2O(g),实验测得:达到平衡状态时,吸收热量19.76KJ.则
①达平衡时混合气体的压强是反应前的
②该条件下的该反应的平衡常数是
③该条件下反应达平衡状态的依据是(填序号)
A.υ正(CH3OH)=υ正(CO2) B.混合气体的密度不变
C.c(CH3OH)=c(H2O) D.混合气体的总物质的量不变
(2)甲、乙两容器体积相等,甲容器通入1mol SO2和1mol O2,乙容器通入1mol SO3和0.5mol O2,发生反应:2SO2(g)+O2(g)═2SO3(g)△H<0,甲、乙起始反应温度相同,均和外界无热量交换,平衡时,甲中SO2的转化率为a,乙中SO3的分解率为b,则a、b的关系为a+b
(3)甲醇是燃料电池的常见原料,现以熔融的K2CO3为电解质,以甲醇为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.如图是甲醇燃料电池模型,试回答下列问题:
①写出该燃料电池的负极反应式
②空气应该从
③如果用该电池作为电解装置,当有16g甲醇发生反应时,则理论上提供的电量最多为(法拉第常数F=9.65×104 C?mol-1)
考点:化学平衡的影响因素,化学电源新型电池,化学平衡的计算
专题:基本概念与基本理论
分析:(1)①恒温恒容下,气体的压强之比等于物质的量之比;
②利用三段式法计算出平衡时的浓度,K=
;
③平衡状态时正逆反应速率相等,各组分的浓度保持不变;
(2)二氧化硫和氧气反应放热,分解三氧化硫吸热,在绝热容器中影响平衡移动;
(3)①结合电解质的成分解答;
②氧气发生还原反应在正极,阴离子移向负极;
③据电极反应式计算.
②利用三段式法计算出平衡时的浓度,K=
| 生成物浓度的幂次方 |
| 反应物浓度的幂次方 |
③平衡状态时正逆反应速率相等,各组分的浓度保持不变;
(2)二氧化硫和氧气反应放热,分解三氧化硫吸热,在绝热容器中影响平衡移动;
(3)①结合电解质的成分解答;
②氧气发生还原反应在正极,阴离子移向负极;
③据电极反应式计算.
解答:
解:(1)①吸热19.76KJ,据方程式可以求得,反应的甲醇有
=0.4mol,则
CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H(298K)=+49.4kJ/mol
反应前(mol) 1 3 0 0
反应了(mol) 0.4 0.4 0.4 1.2
平衡后(mol) 0.6 2.6 0.4 1.2
平衡后,混合气体的压强是原来的
=1.2,
故答案为:1.2;
②K=
=
≈0.11,
故答案为:0.11;
③A、不能体现正逆反应速率相等,故A错误;
B、体积不变,反应物和生成物都是气体,所以密度永远不变,故B错误;
C、甲醇和水蒸气浓度相等,决定于加入的量,与是否平衡无关,故C错误;
D、反应前后气体体积不同,所以气体总物质的量不变说明正逆反应速率相等,反应达到平衡状态,故D正确;
故选D.
(2)若温度和体积都相同时,a+b=1,但现在是绝热容器,甲中温度会升高,抑制了二氧化硫与氧气化合,乙中温度会降低,抑制了三氧化硫的分解,所以,a+b<1,故答案为:<;
(3)①甲醇在负极发生氧化反应,电解质溶液是熔融的K2CO3,所以负极的电极反应式应为:CH3OH-6e-+3CO32-=4CO2+2H2O,
故答案为:CH3OH-6e-+3CO32-=4CO2+2H2O;
②氧气应在正极反应,所以从d口通入,阴离子从右到左移向负极,故答案为:d;从右到左;
③从电极反应式CH3OH-6e-+3CO32-=4CO2+2H2O 可知,1mol甲醇反应转移6mol电子,现在有
=0.5mol甲醇反应,转移电子物质的量为3mol,则理论上提供的电量最多为,3mol×9.65×104 C?mol-1=2.895×105 C,故答案为:2.895×105 C.
| 19.76KJ |
| 49.4KJ/mol |
CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H(298K)=+49.4kJ/mol
反应前(mol) 1 3 0 0
反应了(mol) 0.4 0.4 0.4 1.2
平衡后(mol) 0.6 2.6 0.4 1.2
平衡后,混合气体的压强是原来的
| 0.6+2.6+0.4+11.2 |
| 1+3 |
故答案为:1.2;
②K=
| 生成物浓度的幂次方 |
| 反应物浓度的幂次方 |
| 1.23×0.4 |
| 0.6×2.6 |
故答案为:0.11;
③A、不能体现正逆反应速率相等,故A错误;
B、体积不变,反应物和生成物都是气体,所以密度永远不变,故B错误;
C、甲醇和水蒸气浓度相等,决定于加入的量,与是否平衡无关,故C错误;
D、反应前后气体体积不同,所以气体总物质的量不变说明正逆反应速率相等,反应达到平衡状态,故D正确;
故选D.
(2)若温度和体积都相同时,a+b=1,但现在是绝热容器,甲中温度会升高,抑制了二氧化硫与氧气化合,乙中温度会降低,抑制了三氧化硫的分解,所以,a+b<1,故答案为:<;
(3)①甲醇在负极发生氧化反应,电解质溶液是熔融的K2CO3,所以负极的电极反应式应为:CH3OH-6e-+3CO32-=4CO2+2H2O,
故答案为:CH3OH-6e-+3CO32-=4CO2+2H2O;
②氧气应在正极反应,所以从d口通入,阴离子从右到左移向负极,故答案为:d;从右到左;
③从电极反应式CH3OH-6e-+3CO32-=4CO2+2H2O 可知,1mol甲醇反应转移6mol电子,现在有
| 16g |
| 32g/mol |
点评:本题考查了气体物质的量之比与压强的关系、化学平衡常数的求算、平衡状态的判断、温度对平衡移动的影响、原电池中电极反应式书写、离子移动方向等等,题目有一定难度.

练习册系列答案
相关题目
海水提镁的主要流程如下:

下列说法正确的是( )
①试剂M是盐酸
②流程中的反应全部都是非氧化还原反应
③操作b只是过滤
④用海水晒盐后的饱和溶液加石灰乳制Mg(OH)2
⑤电解熔融MgCl2比电解熔融的MgO制金属镁更节约能量.

下列说法正确的是( )
①试剂M是盐酸
②流程中的反应全部都是非氧化还原反应
③操作b只是过滤
④用海水晒盐后的饱和溶液加石灰乳制Mg(OH)2
⑤电解熔融MgCl2比电解熔融的MgO制金属镁更节约能量.
| A、①②③④⑤ | B、②③ |
| C、④⑤ | D、①④⑤ |
下列反应中,属于非氧化还原反应的是( )
| A、2FeCl3+Cu=2FeCl2+CuCl2 |
| B、Cl2+H2O═HCl+HClO |
| C、4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| D、CaCO3+2HCl=CaCl2+H2O+CO2↑ |
下列关于海水资源综合利用的说法中,正确的是( )
| A、只通过物理变化即可提取海水中的溴单质 |
| B、海水蒸发制海盐的过程只发生化学变化 |
| C、从海水中可以得到NaCl,可电解NaCl溶液制备Na |
| D、利用海水、铝、空气的航标灯是将化学能转化为电能 |

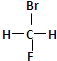 和
和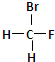 ②1H-、2H、3H+、D2 ③淀粉和纤维素 ④
②1H-、2H、3H+、D2 ③淀粉和纤维素 ④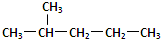 和
和 ⑤16O2、18O3 ⑥235U、238U
⑤16O2、18O3 ⑥235U、238U
 2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心.水是组成生命体的重要化学物质,有关水的反应有很多.
2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心.水是组成生命体的重要化学物质,有关水的反应有很多.