题目内容
按要求书写
(1)H2S的电离方程式
(2)CH3COONa 的电离方程式
(3)泡沫灭火器工作原理的离子方程式
(4)用离子方程式表示纯碱溶液呈碱性的原因 .
(1)H2S的电离方程式
(2)CH3COONa 的电离方程式
(3)泡沫灭火器工作原理的离子方程式
(4)用离子方程式表示纯碱溶液呈碱性的原因
考点:电离方程式的书写,盐类水解的应用
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:(1)H2S是二元弱酸,属弱电解质,分两步电离,第一步电离出氢离子和硫氢根离子,第二步电离:硫氢根离子电离出硫离子和氢离子;
(2)CH3COONa属于强电解质,完全电离出乙酸根离子和钠离子;
(3)硫酸铝和碳酸氢钠相互促进水解生成氢氧化铝和二氧化碳;
(4)碳酸钠是强碱弱酸盐,水溶液中碳酸根离子分步水解,溶液呈碱性.
(2)CH3COONa属于强电解质,完全电离出乙酸根离子和钠离子;
(3)硫酸铝和碳酸氢钠相互促进水解生成氢氧化铝和二氧化碳;
(4)碳酸钠是强碱弱酸盐,水溶液中碳酸根离子分步水解,溶液呈碱性.
解答:
解:(1)H2S是二元弱酸,属弱电解质,分两步电离,第一步电离H2S?H++HS-,第二步电离:HS-?H++S2-,
故答案为:H2S?H++HS-,HS-?H++S2-;
(2)强电解质的电离用“=”,弱电解质的电离用“?”,CH3COONa属于强电解质,完全电离,电离方程式为:CH3COONa═CH3COO-+Na+,
故答案为:CH3COONa═CH3COO-+Na+;
(3)泡沫灭火器中药品是硫酸铝和碳酸氢钠,硫酸铝溶液水解呈酸性,碳酸氢钠溶液水解呈碱性,所以硫酸铝和碳酸氢钠相互促进水解生成氢氧化铝和二氧化碳,其水解方程式为Al3++3HCO3-?Al(OH)3↓+3CO2↑,
故答案为:Al3++3HCO3-?Al(OH)3↓+3CO2↑;
(4)纯碱是强碱弱酸盐,碳酸根离子能发生水解使溶液中的氢氧根离子的浓度大于氢离子的浓度,导致溶液呈碱性,离子方程式为 CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,
故答案为:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-.
故答案为:H2S?H++HS-,HS-?H++S2-;
(2)强电解质的电离用“=”,弱电解质的电离用“?”,CH3COONa属于强电解质,完全电离,电离方程式为:CH3COONa═CH3COO-+Na+,
故答案为:CH3COONa═CH3COO-+Na+;
(3)泡沫灭火器中药品是硫酸铝和碳酸氢钠,硫酸铝溶液水解呈酸性,碳酸氢钠溶液水解呈碱性,所以硫酸铝和碳酸氢钠相互促进水解生成氢氧化铝和二氧化碳,其水解方程式为Al3++3HCO3-?Al(OH)3↓+3CO2↑,
故答案为:Al3++3HCO3-?Al(OH)3↓+3CO2↑;
(4)纯碱是强碱弱酸盐,碳酸根离子能发生水解使溶液中的氢氧根离子的浓度大于氢离子的浓度,导致溶液呈碱性,离子方程式为 CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,
故答案为:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-.
点评:本题考查了电离与水解方程式的书写,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的关键,注意弱电解质的电离、水解均为可逆反应,题目难度不大.

练习册系列答案
相关题目
分子式为C6H12O2的有机物在酸性条件下可水解为酸和醇,且生成的醇没有相同官能团的同分异构体.若不考虑立体异构,这些酸和醇重新组合可形成的酯共有( )
| A、8种 | B、12种 |
| C、24种 | D、28种 |
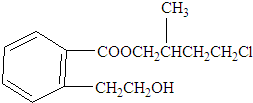 某有机化合物A的结构简式如图
某有机化合物A的结构简式如图
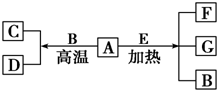 A~G是中学化学常见物质,A、D为单质,G是含A元素的酸性气体.
A~G是中学化学常见物质,A、D为单质,G是含A元素的酸性气体.