题目内容
(12分)(1)某建筑材料,主要成分为铝硅酸盐,化学式是MgAl2H4Si4O14;化学式改写成氧化物形式为_________。该材料与酸或碱反应时可以看作各氧化物分别与酸、碱反应,则材料该与足量的氢氧化钠反应后过滤,滤渣主要是_______。
(2)除去镁粉中混有的铝粉(用离子方程式表示) 。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。原因是 (用化学方程式表式)
(4)向100ml水中投入Na和Al共16克,充分反应后剩余金属1g。则放出H2的体积为 升(标况下)
(5)标准状况下把11.2L氯气通入500ml0.8mol/LFeBr2溶液中,写出反应完全后的离子方程式
(1) MgO·Al2O3·4SiO2·2H2O MgO (2)2Al+2 OH-+2H2O══2AlO2-+3H2↑
(3)4Fe(OH)2+O2+2H2O=4Fe(OH) (4)13.44 (5)(4)5Cl2+4Fe2++6Br=10Cl-+4Fe3++3Br2
【解析】
试题分析:(1)硅酸盐由盐的书写改写为氧化物的形式即改写的一般方法归纳为:碱性氧化物、两性氧化物、酸性氧化物、水(xMO?nSiO2?mH2O),改写成氧化物形式为MgO·Al2O3·4SiO2·2H2O。氧化铝、二氧化硅与氢氧化钠溶液反应,氧化镁与氢氧化钠溶液不反应,滤渣主要是MgO;(2)铝粉可与氢氧化钠反应生成可溶性的偏铝酸钠,然后过滤得到镁,2Al+2 OH-+2H2O══2AlO2-+3H2↑;(3)为避免生成的Fe(OH)2沉淀接触O2,可用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液方可达到目的;(4)Al和水不反应,所以剩余金属应该是Al,反应方程式为2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,可以得出关系式Na~NaOH~Al,则参与反应的Na和Al的质量之比为23:27,Na和Al的质量和为15g,所以n(Na)=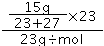 =0.3mol,n(Al)=
=0.3mol,n(Al)=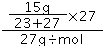 =0.3mol, 根据Na、Al和氢气之间的关系式得氢气体积=(0.3mol×0.5+0.3mol×1.5)×22.4L/mol=13.44L。(5)氯气的物质的量=
=0.3mol, 根据Na、Al和氢气之间的关系式得氢气体积=(0.3mol×0.5+0.3mol×1.5)×22.4L/mol=13.44L。(5)氯气的物质的量=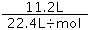 =0.5mol,溴化亚铁的物质的量=0.8mol/L×0.5L=0.4mol,n(Fe2+)=0.4mol,n(Br-)=0.8mol,发生反应为2Fe2++Cl2=2Fe3++3Cl-、Cl2+2Br-=2Cl-+Br2,亚铁离子的还原性大于溴离子,亚铁离子完全反应需要氯气的物质的量为0.2mol,还剩下0.3mol氯气,0.3mol氯气能氧化溴离子的物质的量是0.6mol,所以参加反应的氯气、亚铁离子、溴离子的物质的量之比为0.5mol:0.4mol:0.6mol=5:4:6,则离子反应方程式为:5Cl2+4Fe2++6Br-=10Cl-+4Fe3++3Br2。
=0.5mol,溴化亚铁的物质的量=0.8mol/L×0.5L=0.4mol,n(Fe2+)=0.4mol,n(Br-)=0.8mol,发生反应为2Fe2++Cl2=2Fe3++3Cl-、Cl2+2Br-=2Cl-+Br2,亚铁离子的还原性大于溴离子,亚铁离子完全反应需要氯气的物质的量为0.2mol,还剩下0.3mol氯气,0.3mol氯气能氧化溴离子的物质的量是0.6mol,所以参加反应的氯气、亚铁离子、溴离子的物质的量之比为0.5mol:0.4mol:0.6mol=5:4:6,则离子反应方程式为:5Cl2+4Fe2++6Br-=10Cl-+4Fe3++3Br2。
考点:考查硅酸盐、金属钠镁铝及其化合物的性质、氯气的性质。

 2AB3(g)△H >0下列图象中正确的是
2AB3(g)△H >0下列图象中正确的是 

 H3O++B2–
H3O++B2– H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-