题目内容
10.化学与生产、生活、科技、环境等密切相关,下列说法正确的是( )| A. | 研发使用高效催化剂,可提高反应中原料的转化率 | |
| B. | 铅笔芯的原材料为铅,所以儿童常咬铅笔头容易铅中毒 | |
| C. | 网络飞速发展,得益于光纤良好的导电性,光纤的主要成分是二氧化硅 | |
| D. | 用K2FeO4取代Cl2处理饮用水,不仅可杀菌消毒,同时还能沉降水中的悬浮物 |
分析 A.催化剂能改变反应速率,对化学平衡移动不产生影响;
B.铅笔芯的原材料为碳;
C.二氧化硅具有良好的光学特性,不导电;
D.K2FeO4具有强氧化性,还原产物可水解生成具有吸附性的胶体.
解答 解:A.研发使用高效催化剂,可提高反应速率,不能提高原料的转化率,故A错误;
B.铅笔芯的原材料为碳,不具有毒性,故B错误;
C.二氧化硅不导电,故C错误;
D.K2FeO4具有强氧化性,还原产物可水解生成具有吸附性的胶体,可用于净水,故D正确;
故选:D.
点评 本题考查元素化合物知识,为高频考点,侧重化学与生活、生产等知识,有利于培养学生良好的科学素养,提高学习的积极性,难度不大,注意化学平衡移动影响因素.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
20.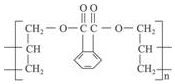 DAP是电器和仪表部件中常用的一种合成髙分子化合物(结构简式如图),合成此该高分子的单体可能是( )
DAP是电器和仪表部件中常用的一种合成髙分子化合物(结构简式如图),合成此该高分子的单体可能是( )
①烯CH2=CH2
②丙烯CH3CH=CH2
③丙烯醇(CH2=CH-CH2OH)
④邻苯二甲酸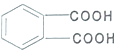
⑤邻苯二甲酸酯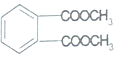
 DAP是电器和仪表部件中常用的一种合成髙分子化合物(结构简式如图),合成此该高分子的单体可能是( )
DAP是电器和仪表部件中常用的一种合成髙分子化合物(结构简式如图),合成此该高分子的单体可能是( )①烯CH2=CH2
②丙烯CH3CH=CH2
③丙烯醇(CH2=CH-CH2OH)
④邻苯二甲酸

⑤邻苯二甲酸酯

| A. | ①② | B. | ③④ | C. | ②④ | D. | ③⑤ |
1.依据元素周期表判断,下列各组关系中正确的是( )
| A. | 稳定性:NH3>H2O>H2S | B. | 氧化性:Cl2>S>P | ||
| C. | 酸性:H3PO4>H2SO4>HClO4 | D. | 碱性:Mg(OH)2>Ca(OH)2>Ba(OH)2 |
18.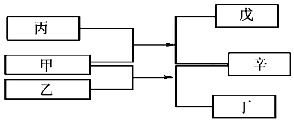 A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )
 A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质,常温常压下乙为液体.常温下,0.1mol/L 丁溶液的pH为13,上述各物质间的转化关系如图所示.下列说法正确的是( )| A. | 元素B、C、D的原子半径由大到小的顺序为 r(D)>r(C)>r(B) | |
| B. | 1L0.lmol/L戊溶液中阴离子的总物质的量小于0.1mol | |
| C. | 1mol甲与足量的乙完全反应共转移了约6.02×1023个电子 | |
| D. | 元素的非金属性B>C>A |
5.“银针验毒”在我国有上千年历史,银针主要用于检验是否有含硫元素的有毒物质.其反应原理之一为:Ag+2H2S+O2→Ag2S+H2O.当银针变色后,将其置于盛有食盐水的铝制容器中一段时间后便可复原.以下说法不正确的是( )
| A. | 当银针变黑时,所检验的物质有毒 | |
| B. | 银针验毒时,Ag被氧化 | |
| C. | 上述验毒反应的氧化产物和还原产物的物质的量之比为1:1 | |
| D. | 银针复原发生的反应可能为:3Ag2S+2Al═6Ag+Al2S3 |
15.已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,其中只有一种金属元素,X是周期表中原子半径最小的元素,Y的最高正价与最低负价绝对值相等,W最外层电子数是最内层电子数的3倍,R是同周期元素中原子半径最小的元素.下列说法不正确的是( )
| A. | 原子半径Z>W>R | |
| B. | 对应的氢化物的热稳定性:R>W>Y | |
| C. | 单质Z可与R的最高价含氧酸发生置换反应 | |
| D. | W与R所形成的简单离子均能影响水的电离平衡 |
2.如图甲是利用一种微生物将废水中的尿素(H2NCONH2)的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中不正确的是( )
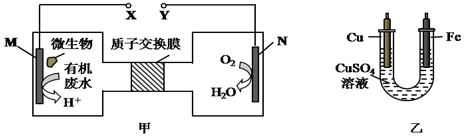

| A. | 铜电极应与Y相连接 | |
| B. | 乙装置中溶液的颜色不会变浅 | |
| C. | 当N电极消耗0.25 mol气体时,则铁电极质量增加16 g | |
| D. | M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ |
19.某老师批阅学生实验报告,下列哪些学生是以科学的态度记录实验数据的( )
| A. | 甲学生用电子天平称取NaOH固体1.220g | |
| B. | 乙学生用广泛pH试纸测定溶液的酸碱性:pH=14.5 | |
| C. | 丙学生用碱式滴定管取25.0mL0.lmol/L的盐酸 | |
| D. | 丁学生用50mL 量筒量取46.70mL浓盐酸 |
20.钴(Co)是重要的稀有金属,在工业和科技领域具有广泛的用途.从某含钴工业废料中回收钴的工艺流程如图:
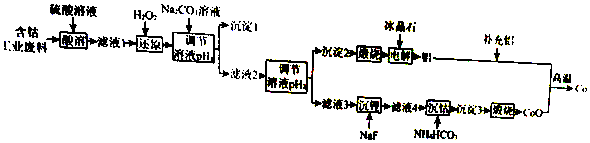
已知:
Ⅲ.离子浓度小于等于1.0×10-5mol•L-1时,认为该离子沉淀完全.
请回答下列问题:
(1)NaF的电子式为Na+[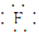 ]-.
]-.
(2)“沉淀1”的化学式为Fe(OH)3.“调节溶液pH2”的范围为4.7≤pH2<7.15.
(3)“还原”时发生反应的离子方程式为2CO3++H2O2=2CO2++O2↑2H+.“沉钴”时发生反应的离子方程式为CO2++2HCO3-=COCO3↓+CO2↑+H2O.
(4)制备Co时,“补充铝”的原因为原混合物中Al和Co的物质的量之比小于2:3.
(5)已知:l0-0.9≈0.13,则 A1(OH)3 的溶度积常数 Ksp=1.3×10-33.
(6)Li-SOCl2电池可用于心脏起搏器,该电池的总反应可表示为::4Li+2SOCl2═4LiCl+S+SO2,其正极反应式为2SOCl2+4e-=S+SO2+4Cl-.

已知:
| 含钴废料的成分 | |||||
| 成分 | Al | Li | Co2O3 | Fe2O3 | 其他不溶于强酸的杂质 |
| 质量分数/% | 10.5 | 0.35 | 65.6 | 9.6 | 13.95 |
| Ⅱ.实验中部分离子开始沉淀和沉淀完全的pH | |||
| 金属离子 | Fe3+ | Co2+ | Al3+ |
| 开始沉淀的pH | 1.9 | 7.15 | 3.4 |
| 沉淀完全的pH | 3.2 | 9.15 | 4.7 |
请回答下列问题:
(1)NaF的电子式为Na+[
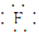 ]-.
]-.(2)“沉淀1”的化学式为Fe(OH)3.“调节溶液pH2”的范围为4.7≤pH2<7.15.
(3)“还原”时发生反应的离子方程式为2CO3++H2O2=2CO2++O2↑2H+.“沉钴”时发生反应的离子方程式为CO2++2HCO3-=COCO3↓+CO2↑+H2O.
(4)制备Co时,“补充铝”的原因为原混合物中Al和Co的物质的量之比小于2:3.
(5)已知:l0-0.9≈0.13,则 A1(OH)3 的溶度积常数 Ksp=1.3×10-33.
(6)Li-SOCl2电池可用于心脏起搏器,该电池的总反应可表示为::4Li+2SOCl2═4LiCl+S+SO2,其正极反应式为2SOCl2+4e-=S+SO2+4Cl-.