题目内容
12.可逆反应H2(g)+I2(g)?2HI(g)达到限度时的标志是( )| A. | 混合气体密度恒定不变 | B. | 消耗n mol H2同时生成2n mol HI | ||
| C. | H2、I2、HI的浓度相等 | D. | 混合气体的颜色不再改变 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、混合气体密度一直不变,故A错误;
B、消耗n mol H2同时生成2n mol HI,都体现的正反应方向,故B错误;
C、当体系达平衡状态时,H2、I2、HI的浓度可能相等,也可能不等,与各物质的初始浓度及转化率有关,故C错误;
D、混合气体的颜色不再改变,说明碘蒸气的物质的量不变,反应达平衡状态,故D正确;
故选D.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
20.下列说法正确的是( )
| A. | 实验室制取乙烯时浓硫酸是催化剂和吸水剂 | |
| B. | 硝基苯制备时浓硫酸作催化剂和脱水剂 | |
| C. | 实验室制备乙烯、硝基苯、苯磺酸时均使用到温度计,且水银球在反应混合物液面以下 | |
| D. | 水浴加热的优点是可以受热均匀且便于控制温度 |
7.下列说法不正确的是( )
| A. | 只用淀粉溶液即可检验食盐是否为加碘盐 | |
| B. | 家庭中不宜用铝合金容器长期存放酸性、碱性或咸的食品 | |
| C. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关 | |
| D. | 用脱硫处理的煤代替原煤作燃料可以有效减少空气中SO2气体的含量 |
4.下列结构简式代表了几种不同的烷烃( )
①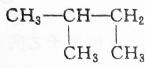
②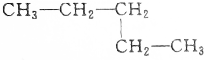
③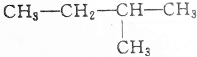
④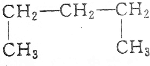
⑤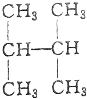
①

②
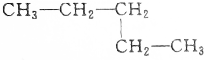
③
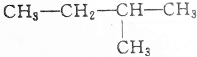
④
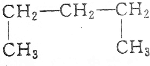
⑤

| A. | 1种 | B. | 2种 | C. | 3种 | D. | 5种 |

 某天然碱样品的组成可能为aNa2CO3•bNaHCO3•cH2O(a、b、c为正整数).为确定其组成,某小组进行如下实验:
某天然碱样品的组成可能为aNa2CO3•bNaHCO3•cH2O(a、b、c为正整数).为确定其组成,某小组进行如下实验: