题目内容
6.有机物 G 是一种医药中间体,常用于制备抗凝血药.可以通过下图所示的路线合成有机物 G.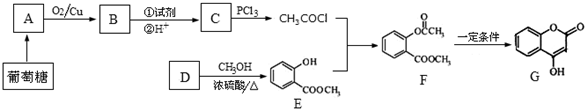
已知:
1.RCOOH$\stackrel{PCl_{3}}{→}$RCOCl
2.
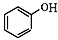 +NaOH→
+NaOH→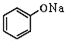 +H2O
+H2O请回答下列问题:
(1)葡萄糖的分子式是C6H12O6,写出 G 中所含含氧官能团的名称羟基、酯基.
(2)由 A 转化为 B 的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(3)已知 D 的分子式为 C7H6O3,则 D 的结构简式为
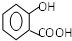 .
.(4)在上述转化过程中,属于取代反应的有②④(填选项序号).
①葡萄糖→A ②D→E ③B→C ④E+CH3COCl→F
(5)写出 F 与足量的氢氧化钠反应生成的有机物的结构简式
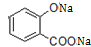 、CH3COONa、CH3OH.
、CH3COONa、CH3OH.
分析 D的分子式为C7H6O3,D与甲醇在浓硫酸存在条件下加热反应生成E,该反应为酯化反应,则D为 ;
;
结合信息RCOOH$\stackrel{PCl_{3}}{→}$RCOCl可知,C与PCl3反应生成CH3COCl,则C的结构简式为:CH3COOH;葡萄糖的分子式为C6H12O,根据葡萄糖→A→B→C的转化条件可知,A被催化氧化成B,B再被氧化成C,所以B的结构简式为:CH3CHO、A为CH3CH2OH;CH3COCl和 反应生成F,F在一定条件下转化成G,据此进行解答.
反应生成F,F在一定条件下转化成G,据此进行解答.
解答 解:D的分子式为C7H6O3,D与甲醇在浓硫酸存在条件下加热反应生成E,该反应为酯化反应,则D为 ;结合信息RCOOH$\stackrel{PCl_{3}}{→}$RCOCl可知,C与PCl3反应生成CH3COCl,则C的结构简式为:CH3COOH;葡萄糖的分子式为C6H12O,根据葡萄糖→A→B→C的转化条件可知,A被催化氧化成B,B再被氧化成C,所以B的结构简式为:CH3CHO、A为CH3CH2OH;CH3COCl和
;结合信息RCOOH$\stackrel{PCl_{3}}{→}$RCOCl可知,C与PCl3反应生成CH3COCl,则C的结构简式为:CH3COOH;葡萄糖的分子式为C6H12O,根据葡萄糖→A→B→C的转化条件可知,A被催化氧化成B,B再被氧化成C,所以B的结构简式为:CH3CHO、A为CH3CH2OH;CH3COCl和 反应生成F,F在一定条件下转化成G,
反应生成F,F在一定条件下转化成G,
(1)葡萄糖的分子式为:C6H12O6;根据G的结构简式可知,G中所含含氧官能图的名称为醛基和酯基,
故答案为:C6H12O6;羟基、酯基;
(2)A为CH3CH2OH,乙醇在催化剂存在条件下可以氧化成乙醛,反应的化学方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(3)根据分析可知,D的结构简式为: ,故答案为:
,故答案为: ;
;
(4)①葡萄糖→A:葡萄糖转化成乙醇为氧化还原反应,不属于取代反应,故①错误;
②D→E: 与甲醇在浓硫酸存在条件下加热反应生成E,该反应为酯化反应,也属于取代反应,故②正确;
与甲醇在浓硫酸存在条件下加热反应生成E,该反应为酯化反应,也属于取代反应,故②正确;
③B→C:乙醛在酸性条件下催化氧化生成乙酸,该反应为氧化反应,故③错误;
④E+CH3COCl→F:CH3COCl和 反应生成HCl和F,该反应为取代反应,故④正确;
反应生成HCl和F,该反应为取代反应,故④正确;
故答案为:②④;
(5)F中有两个酯基与足量NaOH溶液充分反应生成酚羟基也与氢氧化钠反应,所以反应的化学方程式为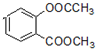 +3NaOH→CH3COONa+CH3OH+
+3NaOH→CH3COONa+CH3OH+ +H2O,则该反应生成的有机物为
+H2O,则该反应生成的有机物为 、CH3COONa、CH3OH,
、CH3COONa、CH3OH,
故答案为: 、CH3COONa、CH3OH.
、CH3COONa、CH3OH.
点评 本题考查有机合成,题目难度中等,解题的关键是利用官能团的性质与转化、结合题中信息进行物质推断,注意熟练掌握常见有机物结构与性质,明确常见有机反应类型及判断方法.

 阅读快车系列答案
阅读快车系列答案| A. | 液氨汽化时吸收大量的热,可用作制冷剂 | |
| B. | 漂白粉和二氧化硫均具有漂白性,将两者混合使用,可增强漂白效果 | |
| C. | 酒精能使蛋白质变性,医院一般用100%的酒精进行消毒 | |
| D. | 氧化铝熔点很高,其制造的坩埚可用于熔融烧碱 |
| A. | 常温常压下,1 L0.1mol•L-1的硝酸铵溶液中氮原子数目为0.2NA | |
| B. | 标准状况下,6.0gNO和2.24LO2混合,所得气体的分子数目为0.2NA | |
| C. | 1 mol有机物 中最多有6 NA个原子在一条直线上 中最多有6 NA个原子在一条直线上 | |
| D. | 1 mol甲基( )所含的电子数为7 NA )所含的电子数为7 NA |
| A. | 油脂、糖类、蛋白质均能在一定条件下发生水解反应 | |
| B. | 乙烯能使溴水、高锰酸钾酸性溶液褪色,且褪色原理相同 | |
| C. | 棉、麻、羊毛、蚕丝均属于天然高分子材料 | |
| D. | 石油的分馏与煤的干馏主要是通过物理变化得到成分不同的有机物 |
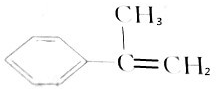 ,则该有机物与氢气完全反应后产物的一氯代物的结构有( )
,则该有机物与氢气完全反应后产物的一氯代物的结构有( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |

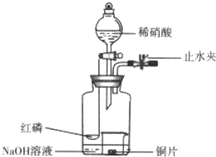 用如图示装置制备NO并验证其还原性.
用如图示装置制备NO并验证其还原性.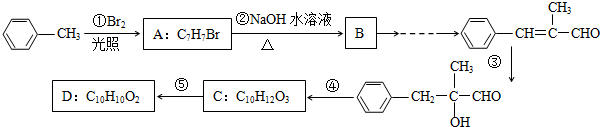

 .
. ,无机试剂任选,格式参照图.
,无机试剂任选,格式参照图. .
.

 .
. .
. .
.
 .
.