题目内容
工业上用铝土矿(主要成分为Al203,还有少量的Fe203、Si02等杂质)提取氧化铝,操作过程如下:

(1)分离溶液和沉淀的操作名称是
(2)沉淀A中主要含有
(3)滤液X中,除了Al3+、H+外,还含有的阳离子是
(4)写出(Ⅲ)步骤反应的化学方程式 ,
(5)Al203属于 氧化物(填“酸性”或“碱性”或“两性”).

(1)分离溶液和沉淀的操作名称是
(2)沉淀A中主要含有
(3)滤液X中,除了Al3+、H+外,还含有的阳离子是
(4)写出(Ⅲ)步骤反应的化学方程式
(5)Al203属于
考点:物质分离和提纯的方法和基本操作综合应用
专题:
分析:铝土矿加入过量盐酸,二氧化硅不反应,沉淀A为Si02,滤液X含有氯化铁、氯化铝等,加入过量氢氧化钠溶液,沉淀B为氢氧化铁,滤液Y含有Na〔Al(OH)4〕,步骤II通入二氧化碳,控制条件使Na〔Al(OH)4〕转化为氢氧化铝沉淀,过滤得氢氧化铝,加热分解氢氧化铝得到氧化铝,滤液Z含有碳酸盐,以此解答该题.
解答:
解:铝土矿加入过量盐酸,二氧化硅不反应,沉淀A为Si02,滤液X含有氯化铁、氯化铝等,加入过量氢氧化钠溶液,沉淀B为氢氧化铁,滤液Y含有Na〔Al(OH)4〕,步骤II通入二氧化碳,控制条件使Na〔Al(OH)4〕转化为氢氧化铝沉淀,过滤得氢氧化铝,加热分解氢氧化铝得到氧化铝,滤液Z含有碳酸盐,
(1)分离溶液和沉淀,可用过滤的防腐,故答案为:过滤;
(2)由以上分析可知沉淀A为Si02,故答案为:Si02;
(3)滤液X中,除了Al3+、H+外,还含有的阳离子是Fe3+,故答案为:Fe3+;
(4)(Ⅲ)为二氧化碳与Na〔Al(OH)4〕转化为氢氧化铝沉淀的反应,化学子方程式为Na〔Al(OH)4〕+CO2═Al(OH)3↓+NaHCO3,
故答案为:Na〔Al(OH)4〕+CO2═Al(OH)3↓+NaHCO3;
(5)Al203可与强酸、强碱反应,为两性氧化物,故答案为:两性.
(1)分离溶液和沉淀,可用过滤的防腐,故答案为:过滤;
(2)由以上分析可知沉淀A为Si02,故答案为:Si02;
(3)滤液X中,除了Al3+、H+外,还含有的阳离子是Fe3+,故答案为:Fe3+;
(4)(Ⅲ)为二氧化碳与Na〔Al(OH)4〕转化为氢氧化铝沉淀的反应,化学子方程式为Na〔Al(OH)4〕+CO2═Al(OH)3↓+NaHCO3,
故答案为:Na〔Al(OH)4〕+CO2═Al(OH)3↓+NaHCO3;
(5)Al203可与强酸、强碱反应,为两性氧化物,故答案为:两性.
点评:本题以工艺流程题形式考查铝的化合物的性质、物质的分离提纯、处于化学用语书写等,难度中等,清楚工艺流程原理是关键,是对知识迁移的综合运用.

练习册系列答案
相关题目
 台湾的食品中“塑化剂”是一种塑料中的添加剂,不是食品添加剂,会危害男性生殖能力,促使女性性早熟,会伤害人类基因.因此不能用于食品当中,而且用了增塑剂的包装材料或者容器不能用于包装脂肪性的食品.有关说法正确的是( )
台湾的食品中“塑化剂”是一种塑料中的添加剂,不是食品添加剂,会危害男性生殖能力,促使女性性早熟,会伤害人类基因.因此不能用于食品当中,而且用了增塑剂的包装材料或者容器不能用于包装脂肪性的食品.有关说法正确的是( )| A、“塑化剂”能溶于水 |
| B、“塑化剂”是邻苯二甲酸酯,它水解可以生成邻苯二甲酸和醇 |
| C、该物质为高分子化合物 |
| D、应推广使用聚氯乙烯塑料袋包装食品 |
能用于鉴别淀粉、肥皂和蛋白质三种溶液的试剂是( )
| A、碘水 | B、硫酸镁溶液 |
| C、烧碱溶液 | D、浓硝酸 |
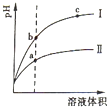 某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断正确的是( )
某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断正确的是( )| A、Ⅱ为盐酸稀释时pH变化曲线 |
| B、导电性:b点>c点 |
| C、Kw的数值:a点>c点 |
| D、酸的总浓度:b点>a点 |

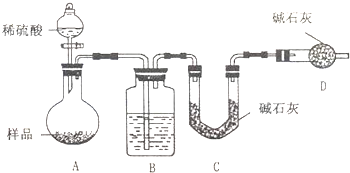
 氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)