题目内容
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: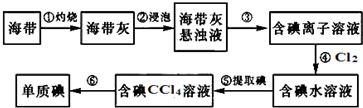
请填写下列空白:
(1)步骤⑤的操作名称是 ,除烧杯外,还必须用到的仪器是:
从碘水溶液中提取碘,还可以选用下列 (填字母)物质作为萃取剂.
A.酒精 B.苯(密度比水小) C.KI溶液
(2)步骤③的实验操作名称是
(3)步骤④中反应的化学方程式是
(4)步骤⑥的目的是从含碘的四氯化碳溶液中分离出单质碘和回收四氯化碳,该步骤的实验操作名称是 .

请填写下列空白:
(1)步骤⑤的操作名称是
从碘水溶液中提取碘,还可以选用下列
A.酒精 B.苯(密度比水小) C.KI溶液
(2)步骤③的实验操作名称是
(3)步骤④中反应的化学方程式是
(4)步骤⑥的目的是从含碘的四氯化碳溶液中分离出单质碘和回收四氯化碳,该步骤的实验操作名称是
考点:海带成分中碘的检验
专题:
分析:(1)根据实验操作步骤⑤提取碘来分析用到的实验仪器;
(2)分离液体与固体的操作是过滤;
(3)氯气的氧化性强于碘单质,故可以利用单质间的置换反应制取碘单质,依据化学反应方程式的书写方法书写即可;
(4)分离碘与四氯化碳溶液利用的两物质沸点的不同,即蒸馏.
(2)分离液体与固体的操作是过滤;
(3)氯气的氧化性强于碘单质,故可以利用单质间的置换反应制取碘单质,依据化学反应方程式的书写方法书写即可;
(4)分离碘与四氯化碳溶液利用的两物质沸点的不同,即蒸馏.
解答:
解:(1)利用碘易溶于有机溶剂的性质来进行提取碘,故此操作为萃取,所需要的仪器为分液漏斗,选择的能提取碘的试剂除了对I2有强的溶解能力处,还必须难溶于水,否则不能进行分液分离,符合条件的是苯,故答案为:B;故答案为:萃取;分液漏斗;B;
(2)步骤③为分离液体和难溶于水的固体,此操作为过滤,故答案为:过滤;
(3)步骤④中是氯气置换KI溶液中的碘离子生成碘单质,化学反应方程式为:Cl2+2KI=2KCl+I2,故答案为:Cl2+2KI=2KCl+I2;
(4)从含碘的四氯化碳溶液中分离出单质碘和回收四氯化碳,应利用沸点的不同分离,故操作为:蒸馏,故答案为:蒸馏.
(2)步骤③为分离液体和难溶于水的固体,此操作为过滤,故答案为:过滤;
(3)步骤④中是氯气置换KI溶液中的碘离子生成碘单质,化学反应方程式为:Cl2+2KI=2KCl+I2,故答案为:Cl2+2KI=2KCl+I2;
(4)从含碘的四氯化碳溶液中分离出单质碘和回收四氯化碳,应利用沸点的不同分离,故操作为:蒸馏,故答案为:蒸馏.
点评:本题考查制备实验方案的设计,分离物质所需要的仪器以及常见实验操作的判断,题目难度不大,注意基本实验操作的要点和注意事项.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
下列物质中,属于能导电的电解质的是( )
| A、无水酒精 |
| B、熔融的氯化钠 |
| C、纯铝导线 |
| D、氢氧化钠晶体 |
 有X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16.X、Y、Z三种元素的常见单质在适当条件下可发生如下变化,其中B和C均为10电子分子.下列说法中不正确的是( )
有X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16.X、Y、Z三种元素的常见单质在适当条件下可发生如下变化,其中B和C均为10电子分子.下列说法中不正确的是( )| A、X元素位于ⅥA |
| B、热稳定性:B>C |
| C、C极易溶于B中,溶液呈碱性 |
| D、A和C不可能发生氧化还原反应 |
下列解释正确的是( )
| A、摩尔是国际七个基本物理量之一 |
| B、物质的量是一个独立的专有名词 |
| C、摩尔是物质的质量的单位 |
| D、摩尔质量等于相对分子质量 |
下列电离方程式错误的是( )
| A、含H2CO3的溶液:H2CO3═2H++CO32- |
| B、极少量Fe(OH)3溶于水:Fe(OH)3?Fe3++3OH- |
| C、醋酸溶液:CH3COOH??H++CH3COO- |
| D、NaHSO4溶于水:NaHSO4═Na++H++SO42- |
将含有硝酸钙和硫酸镁杂质的硝酸钾溶于水,加入某些试剂,结合过滤、蒸发等操作,可得到纯净的硝酸钾.加入试剂的顺序正确的是( )
| A、K2CO3、Ba(NO3)2、KOH、HNO3 |
| B、Ba(NO3)2、KOH、HNO3、K2CO3 |
| C、KOH、K2CO3、Ba(NO3)2、HNO3 |
| D、Ba(NO3)2、KOH、K2CO3、HNO3 |
 在密闭容器中进行如下反应:H2(g)+I2(g)?2HI(g),在温度T1和T2时,产物的量与反应的时间的关系如图所示符合图示的正确判断是( )
在密闭容器中进行如下反应:H2(g)+I2(g)?2HI(g),在温度T1和T2时,产物的量与反应的时间的关系如图所示符合图示的正确判断是( )| A、T1>T2,△H>0 |
| B、T1<T2,△H<0 |
| C、T1<T2,△H>0 |
| D、T1>T2,△H<0 |