题目内容
6.化学是一门实用性很强的科学,与社会、环境等密切相关.下列说法错误的是( )| A. | “静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量 | |
| B. | 雾霾可能是许多细小液体小液滴和固体小颗粒分散到空气中形成的一种胶体 | |
| C. | 铝制餐具不宜用来蒸煮或长时间存放咸的食品 | |
| D. | 在食品袋中放入CaCl2•6H2O,可防止食物受潮 |
分析 A.“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”能够减少空气污染物的排放;
B.如粒子直径介于1-100nm之间,则属于胶体;
C.铝制餐具中含有杂质,比如碳,与氯化钠溶液接触时,就会形成原电池;
D.CaCl2•6H2O不具有吸水性.
解答 解:A.“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”能够减少空气污染物的排放,有利于提高空气质量,故A正确;
B.细小液体小液滴和固体小颗粒分散到空气中,如粒子直径介于1-100nm之间,则属于胶体,故B正确;
C.铝制餐具中含有杂质,比如碳,当这样有杂质的表面与氯化钠溶液接触时,就会形成原电池,铝失电子产生铝离子,人体摄入过量的铝有害,故C正确;
D.CaCl2•6H2O不具有吸水性,不能用于食品防潮,应用无水氯化钙,故D错误;
故选D.
点评 本题综合考查物质的组成、性质与应用,为高考常见题型,侧重于化学与生活、化学与环境的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
相关题目
16.关于元素周期表中的17号元素的说法不正确的是( )
| A. | 最高正价是+7价 | B. | 最低负价为-1价 | ||
| C. | 该元素位于第二周期 | D. | 该元素属于ⅦA族元素 |
17.下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 测定等浓度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者大 | 非金属性:S>C |
| B | 滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 不能确定原溶液中 含NH4+ |
| C | 将HI溶液与CC14溶液在试管中混合,加入 Fe(NO3)3溶液,振荡,静置 | 下层液体显紫红色 | 氧化性:Fe3+>I2 |
| D | 将淀粉溶液与少量稀硫酸混合加热,然后加入新制的Cu(OH)2,悬浊液,并加热 | 无砖红色沉淀 | 淀粉未发生水解 |
| A. | A | B. | B | C. | C | D. | D |
14.化学在人类生活中扮演重要角色,下列说法正确的是( )
| A. | 蔬菜和粗粮中富含纤维素,纤维素在人体中酶的作用下能水解成葡萄糖 | |
| B. | 混凝法、中和法、沉淀法、氧化还原法是工业处理废水常用的方法 | |
| C. | 可只用淀粉溶液检验食盐中是否加碘 | |
| D. | 鸡蛋清溶液中加人饱和Na2SO4溶液,有沉淀生成是因为蛋白质变性 |
1.设NA为阿佛加德罗常数的值,下列叙述正确的是( )
| A. | 11 g由31H和168O组成的超重水中,含有的中子数目为5 NA | |
| B. | 1 molN2与4 mol H2反应生成的NH3分子数为2NA | |
| C. | 过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.2NA | |
| D. | 0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA |
11.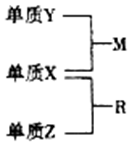 X、Y、Z是短周期元素,原子半径的大小:r(Y)>r(X)>r(Z),三种元素的原子序数之和为15;X、Y、Z三种元素的常见单质在适当条件下可发生如图所示转化关系,其中R为10电子分子,是一种常见的无机溶剂.下列说法不正确的是( )
X、Y、Z是短周期元素,原子半径的大小:r(Y)>r(X)>r(Z),三种元素的原子序数之和为15;X、Y、Z三种元素的常见单质在适当条件下可发生如图所示转化关系,其中R为10电子分子,是一种常见的无机溶剂.下列说法不正确的是( )
 X、Y、Z是短周期元素,原子半径的大小:r(Y)>r(X)>r(Z),三种元素的原子序数之和为15;X、Y、Z三种元素的常见单质在适当条件下可发生如图所示转化关系,其中R为10电子分子,是一种常见的无机溶剂.下列说法不正确的是( )
X、Y、Z是短周期元素,原子半径的大小:r(Y)>r(X)>r(Z),三种元素的原子序数之和为15;X、Y、Z三种元素的常见单质在适当条件下可发生如图所示转化关系,其中R为10电子分子,是一种常见的无机溶剂.下列说法不正确的是( )| A. | X元素位于周期表中的第16列 | |
| B. | X的氢化物沸点一定高于Y的氢化物的沸点 | |
| C. | X、Y、Z元素可以组成一种分子式为Z2Y2X4的化合物,其水溶液中水的电离受到了抑制 | |
| D. | X、Y、Z元素两两之间均能形成原子个数比为1:1的化合物 |
18.下列离子方程式书写正确的是( )
| A. | 在氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 钠投入水中:Na+H2O═Na++2OH-+H2↑ | |
| C. | 氯气和冷的氢氧化钠溶液反应:2Cl2+2OH-═3Cl-+ClO-+H2O | |
| D. | 石灰石加入硝酸溶液中:2H++CO32-═CO2↑+H2O |
10.设NA为阿伏伽徳罗常数的值.下列有关叙述错误的是( )
| A. | 100g质量分数为46%的乙醇水溶液中氧原子数为4NA | |
| B. | lmolCl2通入水中,HC1O、Cl-、ClO-粒子数之和等于2NA | |
| C. | 标准状况下,2.24LD2中所含中子的数目是0.2NA | |
| D. | 25°C时,Ksp(BaSO4)=1×10-10,则 BaSO4饱和溶液中Ba2+浓度为 l×10-5mol•L-1 |