题目内容
下列有关热化学方程式的叙述正确的是( )
| A、已知2H2 (g)+O2(g)═2H2O(g)△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol |
| B、含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4kJ/mol |
| C、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| D、已知C (s)+O2(g)═CO2(g)△H1;C(s)+1/2 O2(g)═CO(g)△H2,则△H1>△H2 |
考点:热化学方程式
专题:化学反应中的能量变化
分析:A、从燃烧热的定义来判断,燃烧热必须是生成稳定的氧化物.
B、从中和热的定义来判断,中和热的热化学方程式必须让生成的水为1mol.
C、从反应的吸放热角度能判断出石墨和金刚石的能量的高低,从而比较出稳定性.
D、比较反应热的大小时要带着正负号比较.
B、从中和热的定义来判断,中和热的热化学方程式必须让生成的水为1mol.
C、从反应的吸放热角度能判断出石墨和金刚石的能量的高低,从而比较出稳定性.
D、比较反应热的大小时要带着正负号比较.
解答:
A、燃烧热指的是在25摄氏度,101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量.定义要点:物质必须是完全燃烧生成稳定的氧化物,即反应物中C→CO2,H2→H2O(l),S→SO2(g).故241.8kJ/mol不是氢气的燃烧热.故A错误.
B、在稀溶液中,酸跟碱发生中和反应生成1 mol水时的反应热叫做中和热中和热.20.0gNaOH的物质的量n=
=
=0.5nol,与稀盐酸完全中和生成0.5mol水,此时放出热量28.7kJ,故当生成1mol水时放热57.4KJ,故该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4kJ/mol,B正确.
C、由C(石墨,s)═C(金刚石,s)△H>0,可知反应吸热,即石墨的能量低于金刚石,而能量越低物质越稳定,故石墨比金刚石稳定,故C错误.
D、反应 C(s)+O2(g)═CO2(g)△H1 ①和反应 C(s)+1/2 O2(g)═CO(g)△H2 ②均为放热反应,△H均小于0.
由于反应①是碳的完全燃烧,②是碳的不完全燃烧,故①放出的热量多于②,则△H1<△H2.故D说法正确.
故选B.
B、在稀溶液中,酸跟碱发生中和反应生成1 mol水时的反应热叫做中和热中和热.20.0gNaOH的物质的量n=
| m |
| M |
| 20g |
| 40g/mol |
C、由C(石墨,s)═C(金刚石,s)△H>0,可知反应吸热,即石墨的能量低于金刚石,而能量越低物质越稳定,故石墨比金刚石稳定,故C错误.
D、反应 C(s)+O2(g)═CO2(g)△H1 ①和反应 C(s)+1/2 O2(g)═CO(g)△H2 ②均为放热反应,△H均小于0.
由于反应①是碳的完全燃烧,②是碳的不完全燃烧,故①放出的热量多于②,则△H1<△H2.故D说法正确.
故选B.
点评:本题考查了燃烧热的概念、中和热的计算以及反应热的大小比较,较简单.

练习册系列答案
相关题目
下列对铯及其化合物的预测正确的是( )
| A、铯的熔点很高 |
| B、在自然界中,铯能以游离态存在 |
| C、氯化铯易溶于水 |
| D、铯只有一种氧化物Cs2O |
根据相应的图象(图象编号与答案对应),判断下列相关说法正确的是( )
A、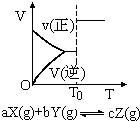 密闭容器中反应达到平衡,t0时改变某一条件有如图变化所示,则改变的条件一定是加入催化剂 |
B、 反应达到平衡时,外界条件对平衡影响关系如图所示,则正反应为放热反应, 且a>b |
C、 物质的百分含量和温度关系如图所示,则该反应的正反应为吸热反应 |
D、 反应速率和反应条件变化关系如图所示,则该反应的正反应为放热反应,A、B、C是气体、D为固体或液体 |
将1.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,一定条件下发生反应:PCl3(g)+Cl2(g)?PCl5(g),达到平衡时PCl5为0.3mol?L-1,如果此时再充入1.0molPCl3和1.0mol Cl2,在相同温度下再达到平衡时,PCl5的物质的量浓度是( )
| A、0.6mol?L-1 |
| B、大于0.3 mol?L-1,小于0.6 mol?L-1 |
| C、大于0.6 mol?L-1 |
| D、小于0.3 mol?L-1 |
某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 如图表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )


| A、t3 时减小了压强 |
| B、t5 时增大了压强 |
| C、t6 时刻后反应物的转化率最高 |
| D、t1-t2 时该反应的平衡常数大于t6时反应的平衡常数 |
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )


| A、图Ⅰ配制1mol/L NaCl溶液定容操作 |
| B、图Ⅱa口进气可收集Cl2、CO2等气体 |
| C、图Ⅲ探究NaHCO3的热稳定性 |
| D、图Ⅳ蒸发结晶获得氯化钠晶体 |
关于化学反应与能量的说法正确的是( )
| A、燃烧属于放热反应 |
| B、反应物总能量与生成物总能量一定相等 |
| C、形成化学键时吸收能量 |
| D、中和反应是吸热反应 |
下列反应是吸热反应的是( )
| A、氢气燃烧 |
| B、NaOH与HCl |
| C、生石灰与水 |
| D、Ba(OH)2?8H2O与NH4Cl |
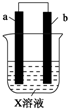 下列对如图所示装置实验判断的描述正确的是( )
下列对如图所示装置实验判断的描述正确的是( )