题目内容
11.下列各组离子,在强酸性溶液中可以大量共存的是( )| A. | Mg2+、Fe3+、SCN-、Cl- | B. | Na+、K+、NO3-、Ba2+ | ||
| C. | Na+、K+、HCO3-、Cl- | D. | Fe2+、Ag+、I-、Cl- |
分析 强酸性溶液中存在大量氢离子,
A.铁离子与硫氰根离子发生反应;
B.四种离子之间不反应,都不与氢离子反应;
C.碳酸氢根离子与氢离子反应;
D.银离子与氯离子反应生成氯化银沉淀.
解答 解:强酸性溶液中存在大量氢离子,
A.Fe3+、SCN-之间发生反应,在溶液中不能大量共存,故A错误;
B.Na+、K+、NO3-、Ba2+之间不发生反应,都不与氢离子反应,在溶液中能够大量共存,故B正确;
C.HCO3-与氢离子反应,在溶液中不能大量共存,故C错误;
D.Ag+、Cl-之间反应生成氯化银沉淀,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-.

练习册系列答案
相关题目
1.下列说法不正确的是( )
| A. | 核磁共振氢谱不能区分CH3CH2OH和CH3OCH3 | |
| B. | 用溴水可以鉴别苯酚溶液、2,4-己二烯和甲苯 | |
| C. | 室温下,在水中的溶解度:甘油>苯酚>溴乙烷 | |
| D. | 两种二肽互为同分异构体,二者的水解产物可能相同 |
19.下列含氧酸中,酸性最弱的是( )
| A. | HClO | B. | HNO2 | C. | H2CO3 | D. | HIO4 |
6.下列变化中,不属于化学变化的是( )
| A. | 新制氯水使有色布条褪色 | B. | 过氧化钠使某些染料褪色 | ||
| C. | Na2O溶于水 | D. | 活性炭使红墨水褪色 |
16.由两种单体加聚而成的高聚物是( )
| A. | 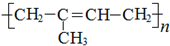 | B. | 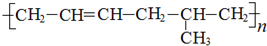 | ||
| C. | 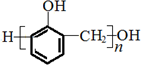 | D. | 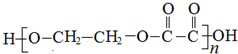 |
3.下列表示物质用途的化学方程式不正确的是( )
| A. | 用硅酸钠与盐酸反应制备硅胶:SiO32-+2H+═H2SiO3(胶体) | |
| B. | 用二氧化硅与烧碱反应制备硅酸钠:SiO2+OH-═SiO32-+H2O | |
| C. | 用铝热法炼铁:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | |
| D. | 用氯气制备漂白粉:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O |
20.用己知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作中正确是( )
| A. | 滴定前,没有逐出滴定管下口的气泡 | |
| B. | 用甲基橙作指示剂,指示剂刚变色,就停止滴定 | |
| C. | 酸式滴定管用蒸馏水洗净后,直接加入己知浓度的盐酸 | |
| D. | 锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液 |
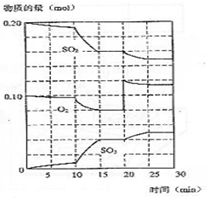 在一定条件下发生如下反应:2SO2(g)+O2 (g)?2SO3(g);△H<0
在一定条件下发生如下反应:2SO2(g)+O2 (g)?2SO3(g);△H<0