题目内容
6.有以下四种微粒14N、15N、N2、N4(结构为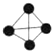 ),已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,下列说法正确的是( )
),已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,下列说法正确的是( )| A. | 14N2与15N2互为同位素,N4与N2互为同素异形体 | |
| B. | N4属于一种新型的化合物 | |
| C. | 14N与15N化学性质不相同 | |
| D. | 1mol N4气体完全转变为N2将放出882kJ热量 |
分析 A.同位素是质子数相同,中子数不同的原子;同素异形体是同种元素形成的不同单质;
B.化合物是由不同种元素组成的纯净物,单质是由同种元素组成的纯净物;
C.同位素化学性质相同;
D.根据化学键断裂要吸收热量,形成化学键要放出热量,根据题中数据计算出1molN4转变成N2放出的热量.
解答 解:A.N4与N2是同种元素形成的不同单质,不是同位素,故A错误;
B.N4由N组成,是一种单质,故B错误;
C.14N与15N互为同位数,化学性质相同,故C错误;
D.1molN4气体中含有0.6molN-N键,可生成2molN2,形成2molN≡N键,则1moN4气体转变为N2化学键断裂断裂吸收的热量为6×167KJ=1002KJ,形成化学键放出的热量为2×942kJ=1884KJ,所以反应放热,放出的热量为1884KJ-1002KJ=882KJ,故应为放出882KJ热量,故D正确;
故选D.
点评 本题考查较为综合,涉及物质的组成和分类以及反应热的计算等问题,题目难度不大,注意基础知识的把握.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
17.下列有关原电池的判断错误的是( )
①所有金属都能作电极
②有活泼性不同的两种金属电极、有电解质溶液、导线就一定能构成原电池,对外放电
③原电池放电实现化学能转化为电能
④以锌、铜为电极,在稀硫酸溶液中构成原电池,正极反应式为Zn-2e-═Zn2+.
①所有金属都能作电极
②有活泼性不同的两种金属电极、有电解质溶液、导线就一定能构成原电池,对外放电
③原电池放电实现化学能转化为电能
④以锌、铜为电极,在稀硫酸溶液中构成原电池,正极反应式为Zn-2e-═Zn2+.
| A. | ①② | B. | ①③ | C. | ①②④ | D. | ①②③④ |
14.下列实验对应的结论不正确的是( )
| A. | 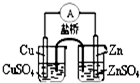 能组成Zn、Cu原电池 | B. |  能证明非金属性C>Si | ||
| C. | 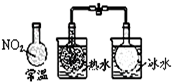 说明反应2NO2?N2O4△H>0 | D. | 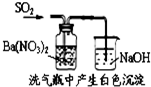 白色沉淀为BaSO4 |
15.100mL 6mol•L-1的H2SO4跟过量锌粉反应,在一定温度下,要想减缓反应进行的速率,但又不影响生成的氢气的总量,可向反应物中加入适量的( )
| A. | 适量浓H2SO4 | B. | 硫酸钾固体 | C. | 醋酸钠固体 | D. | 硝酸钾溶液 |
16.下列有关粒子的表示方法正确的是( )
| A. | 氨气分子的电子式: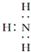 | B. | 硫原子结构示意图: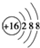 | ||
| C. | 次氯酸的结构式:H-O-Cl | D. | H2O的电子式: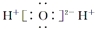 |
 (3)镁离子Mg2+(4)硫离子
(3)镁离子Mg2+(4)硫离子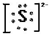 .
.