题目内容
12.乙醚是化工生产中重要的溶剂,也用作药物生产的萃取剂和医疗上的麻醉剂.实验室通过乙醇脱水制备:【原理】2CH3CH2OH$→_{140℃}^{浓硫酸}$CH3CH2OCH2CH3+H2O (170℃时产生CH2=CH2,长时间加热还会发生脱水、氧化还原反应等)
【主要物质物理性质】
| 物质 | 熔点℃ | 沸点℃ | 溶解性 | ||
| 水 | 醇 | 醚 | |||
| 浓H2SO4 | 10.35 | 340 | 互溶 | 互溶 | 互溶 |
| 乙醚 | -89.12 | 34.5 | 微溶(在盐溶液中溶解度降低) | 互溶 | 互溶 |
| 乙醇 | -114.5 | 78.4 | 极易溶 | 极易溶 | 极易溶 |
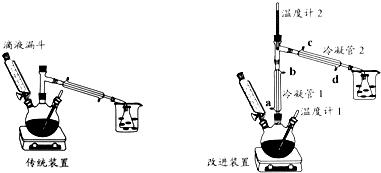
【实验步骤】
I、加浓硫酸和95%乙醇各12mL于三颈瓶中,并将三颈瓶浸入冰水中冷却,将25mL95%乙醇加入滴液漏斗,组装好仪器.
Ⅱ、加热三颈瓶,使反应瓶温度迅速上升到140℃,然后开始慢慢滴加乙醇,控制合适的滴加速度,维持反应温度在135~145℃.
Ⅲ、反应停止后,去掉热源,得粗产品.
Ⅳ、将粗产品转入仪器A,依次用8mL5%NaOH溶液、8mL试剂B、8mL(两次)饱和CaCl2溶液洗涤.
Ⅴ、处理后的粗产品最后用无水氯化钙干燥至澄清,经操作C得到16.8g乙醚.
请回答:
(1)在步骤I中,向三颈瓶中加乙醇和浓硫酸的顺序是先加乙醇,再加浓硫酸.
(2)比较改进装置中两根冷凝管中水温的高低,如果用橡皮管将一个冷凝管的出水口接到另外一个冷凝管的进水口,有关说法和操作方法最合理的是B.
A、冷凝管1的水温相对高,水流方向为a→b→d→c
B、冷凝管1的水温相对高,水流方向为d→c→a→b
C、冷凝管2的水温相对高,水流方向为a→b→d→c
D、冷凝管2的水温相对高,水流方向为d→c→a→b
(3)反应过程中发现温度计1正常,温度计2的读数比预计温度高,为保证实验成功,可进行的操作是D.
A、适当加快滴液漏斗中乙醇的滴加速度
B、降低加热装置的加热温度
C、将温度计2拔高一点
D、加快冷凝管中水的流速
(4)改进装置能将产率提高50%,传统装置产率低的主要原因是传统装置中乙醇被大量蒸出,降低了产率.
(5)在步骤IV中,仪器A的名称是分液漏斗.
(6)在步骤IV中,用NaOH溶液时为了除去二氧化硫、二氧化碳,然后用试剂B洗涤NaOH,以免跟CaCl2产生沉淀,试剂B最好是饱和NaCl溶液(“乙醇”、“蒸馏”、“饱和NaCl”溶液).
分析 (1)根据浓硫酸的稀释操作进行解答;
(2)改进装置提高乙醇的利用率,冷凝管1冷却乙醇,不冷却乙醚,冷凝管2冷却乙醚,乙醇的沸点高于乙醚,则冷凝管1中的温度较高,冷凝管2中的温度较低,结合采取逆流原理通入冷凝水,使冷凝管充满冷凝水,充分冷却;
(3)温度计2的读数比预计温度高,可能有乙醇蒸出,冷凝水未能充分冷却,应加快冷凝管中水的流速;
(4)传统装置中乙醇被蒸出;
(5)粗产品洗涤后需要进行分液分离;
(6)会反应副反应生成二氧化硫、二氧化碳,用NaOH溶液时为了除去二氧化硫、二氧化碳,然后饱和NaCl溶液洗涤NaOH,以免跟CaCl2产生沉淀,可以降低乙醚的溶解度.
解答 解:(1)向三颈瓶A加乙醇和浓硫酸的顺序为:先加入乙醇,再慢慢倒入浓硫酸,边倒边搅拌,
故答案为:乙醇;浓硫酸;
(2)改进装置提高乙醇的利用率,冷凝管1冷却乙醇,不冷却乙醚,冷凝管2冷却乙醚,乙醇的沸点高于乙醚,则冷凝管1中的温度较高,冷凝管2中的温度较低,结合采取逆流原理通入冷凝水,使冷凝管充满冷凝水,充分冷却,水流方向为d→c→a→b,
故选:B;
(3)温度计2的读数比预计温度高,可能有乙醇蒸出,冷凝水未能充分冷却,应加快冷凝管中水的流速,
故选:D;
(4)传统装置中乙醇被大量蒸出,降低了产率,
故答案为:传统装置中乙醇被大量蒸出,降低了产率;
(5)粗产品洗涤后需要进行分液分离,仪器A为分液漏斗,
故答案为:分液漏斗;
(6)会反应副反应生成二氧化硫、二氧化碳,用NaOH溶液时为了除去二氧化硫、二氧化碳,用饱和氯化钠水溶液洗涤,以免跟CaCl2产生沉淀,既可以洗去残留在乙醚中的碱,又可以减少乙醚在水中的溶解度.
故答案为:除去二氧化硫、二氧化碳;饱和NaCl溶液.
点评 本题考查有机物的制备实验,涉及对装置与原理的分析评价、物质的分离提纯等,是对基础知识的综合考查,需要学生具备扎实的基础与分析处理问题的能力.

(1)下列有关滴定操作的顺序正确的是B
①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液 ③检查滴定管是否漏水 ④滴定 ⑤洗涤
A.⑤①②③④B.③⑤①②④C.③⑤②①④D.②①③⑤④
(2)用标准的盐酸滴定待测的NaOH溶液时,一手握酸式滴定管的活塞,一手摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,本实验滴定达到终点的标志是溶液颜色由黄色突变为橙色,且半分钟内不变色
(3)下列哪些操作会使测定结果偏高ABC
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后未用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数仰视滴定管读数,滴定后俯视滴定管读数
(4)某学生根据3次实验分别记录有关数据如下表:
| 滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0mol•L-1盐酸的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 20.00 | 0.00 | 22.20 |
| 第二次 | 20.00 | 1.56 | 25.50 |
| 第三次 | 20.00 | 0.22 | 22.48 |
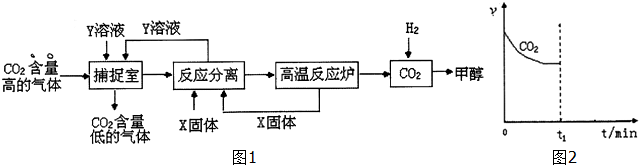
(1)下列有关捕捉空气中的CO2过程中的叙述不正确的有BD.
A、X选用CaO,而且要循环利用CaO与Y溶液
B、捕捉室里温度越高越有利于CO2 的捕捉
C、开放高效光催化剂分解水制氢气,是降低合成甲醇成本的有效途径
D、该捕捉CO2技术的应用有利于缓解全球变暖,而且能耗小
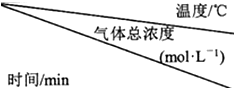
(2)在捕捉室用稀氨水喷淋“捕捉”空气中的CO2时,有NH2COONH4(氨基甲酸胺)生成.现将一定量纯净的氨基甲酸胺置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使反应
NH2COONH4(s)?2NH3(g)+CO2(g)达到分解平衡.实验测得不同温度及反应时间(t1<t2<t3)的有关表:氨基甲酸铵分解时温度、气体总浓度及反应时间的关系
 | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 0.9×10-3 | 2.7×10-3 | 8.1×10-3 |
| t2 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
| t3 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
②根据表中数据换算出,15℃时合成反应2NH3(g)+CO2(g)?NH2COONH4(s)平衡常数K约为4.9×108.
(3)以捕捉到的CO2与H2为原料可合成甲醇(CH3OH),其反应的化学方程为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H<0.
①将1mol CO2和3mol H2充入恒温恒压的密闭容器中发生上述反应,CO2消耗速率v(CO2)与时间关系如图2所示.若在时间t1时,向容器中再充入1mol CO2和3mol H2,请在图中画出CH3OH生成速率v(CH3OH)与时间的关系曲线.
②在一个恒温固定容积的密闭容器中,加入1mol CO2和3mol H2,充分反应后达到平衡放出热量为aKJ.若在原来的容器中加入2mol CO2和6mol H2,在相同温度下充分反应,达到平衡放出热量为bKJ.则a和b满足的关系b>2a.
| A. | 合金的熔点一般比组分金属高 | B. | 合金中只含金属元素 | ||
| C. | 合金的机械性能一般比组分金属好 | D. | 合金的硬度一般比组分小 |
| A. | 同时生成的气体是氧气 | |
| B. | 氧化剂是氢氧化钠和水 | |
| C. | 当产生1.5mol气体时电子转移3NA个 | |
| D. | 这个反应体现了金属的通性 |
| A. | SO2、CO2性质相似,都能在水溶液中被氯气氧化 | |
| B. | Na2O2、Na2O组成元素相同,与CO2反应产物也相同 | |
| C. | Mg和K在一定条件下与水反应都生成H2和对应的碱 | |
| D. | Na、Li同属于碱金属单质,在加热条件下与氧气反应都生成过氧化物 |

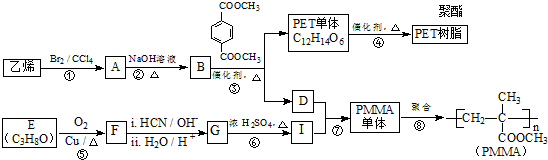
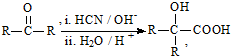 (R、R′代表烃基)
(R、R′代表烃基) .
. .
. .
.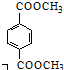 与足量NaOH溶液反应时,最多消耗4molNaOH
与足量NaOH溶液反应时,最多消耗4molNaOH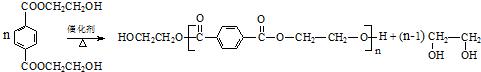 .
.