题目内容
6.AgNO3的水溶液呈酸(填“酸”、“中”、“碱”)性,常温时的pH<7(填“>”、“=”、“<”),原因是(用离子方程式表示):Ag++H2O?AgOH+H+;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以抑制(填“促进”、“抑制”)其水解.分析 AgNO3是强酸弱碱盐,银离子水解导致溶液呈酸性,常温下pH<7,为防止AgNO3水解,所以配制AgNO3溶液时将AgNO3先溶于较浓的硝酸中,然后稀释,据此分析解答.
解答 解:AgNO3是强酸弱碱盐,银离子水解方程式为Ag++H2O?AgOH+H+,水解后溶液中c(H+)>c(OH-),所以溶液呈酸性,即常温下pH<7;为防止AgNO3水解,应该向溶液中加入少量酸,所以配制AgNO3溶液时将AgNO3先溶于较浓的硝酸中,然后稀释,
故答案为:酸;<;Ag++H2O?AgOH+H+;抑制.
点评 本题考查盐类水解,根据盐类水解特点“谁强谁显性、谁弱谁水解、强强显中性”确定溶液酸碱性,会正确书写水解方程式,题目难度不大.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
17.下列实验操作中,错误的是( )
| A. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球位于蒸馏烧瓶支管处 | |
| C. | 萃取时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| D. | 蒸发时,蒸发皿中出现大量固体时即停止加热 |
1.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ | |
| B. | 无色溶液中:K+、Fe3+、SO42-、H+ | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012 的溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | 由水电离的c (H+)=1×10一14 mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
11.下列溶液中有关物质的量浓度关系正确的是( )
| A. | Na2S 溶液中 c(OH-)=c(H+)+c(HS-)+2c(H2S) | |
| B. | Na2CO3溶液中:c(Na+)=2c(CO32-)+2c(HCO3-) | |
| C. | 室温下,pH=1的CH3COOH溶液和pH=13的NaOH溶液等体积混合:溶液中离子浓度的大小顺序为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 0.1mol•L-1的NaHC2O4溶液的pH=4,则c(H C2O4-)>c(H+)>c(H2C2O4)>c(C2O42-) |
18.下列自然、生活中的事例不属于氧化还原反应的是( )
| A. | 食物腐败 | B. | 植物光合作用 | C. | 金属生锈 | D. | 石膏点制豆腐 |
15.下列关于氯气的说法不正确的是( )
| A. | 氯气和液氯是两种不同的物质 | |
| B. | 可以用浓硫酸除去氯气中的水蒸气 | |
| C. | 氯气是一种有毒气体,但可用于自来水的杀菌消毒 | |
| D. | 尽管氯气的化学性质很活泼,但是纯净的液氯能用钢瓶贮存 |
17.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1个甲烷(CH4)分子中有4个C-H键 | |
| B. | 同温、同压下,相同体积的氟气和氢气所含的原子数相等 | |
| C. | 标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA | |
| D. | 在含2molH2SO4的浓H2SO4溶液中加入足量的Zn粉,使其充分反应,则反应结束时转移电子数共4NA(Zn+2H2SO4(浓)→ZnSO4+SO2↑+H2O) |
 氮是动植物生长不可缺少的元素,含氮化合物也是重要的化工原料.自然界中存在如下氮的循环过程,工业上也可通过一系列的化学反应模拟该过程,实现氮的转化.
氮是动植物生长不可缺少的元素,含氮化合物也是重要的化工原料.自然界中存在如下氮的循环过程,工业上也可通过一系列的化学反应模拟该过程,实现氮的转化.
 ;
;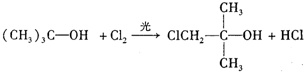 ,反应类型:取代反应;
,反应类型:取代反应; .
.