题目内容
10.根据下面的四个装置图判断下列说法不正确的是( )| A. | 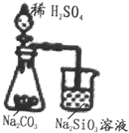 可以用业证明非金属性的相对强弱S>C>Si 可以用业证明非金属性的相对强弱S>C>Si | |
| B. | 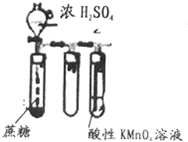 可以用来检验是否有还原性气体生成 可以用来检验是否有还原性气体生成 | |
| C. | 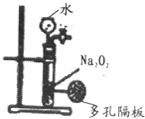 该装置可以用业制备少量氧气,且可以控制反应的进行及快慢 该装置可以用业制备少量氧气,且可以控制反应的进行及快慢 | |
| D. |  滴定过程中褪色速度由慢到快又减慢,达到终点时,溶液的颜色从无色突变为浅紫红色 滴定过程中褪色速度由慢到快又减慢,达到终点时,溶液的颜色从无色突变为浅紫红色 |
分析 A.发生强酸制取弱酸的反应;
B.还原性气体能使高锰酸钾溶液褪色;
C.过氧化钠为粉末固体;
D.高锰酸钾溶液为紫红色.
解答 解:A.发生强酸制取弱酸的反应,则酸性为硫酸>碳酸>硅酸,则非金属性为S>C>Si,故A正确;
B.还原性气体能使高锰酸钾溶液褪色,反应生成二氧化硫,可褪色,故B正确;
C.过氧化钠为粉末固体,关闭止水夹不能使反应停止来制备少量氧气,故C错误;
D.高锰酸钾溶液为紫红色,滴定终点时,溶液的颜色从无色突变为浅紫红色,故D正确.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及酸性和非金属性比较、气体的制备和收集、中和滴定等,把握物质的性质及实验原理为解答的关键,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
16.某烃的一种同分异构体的 1H核磁共振谱图只有一组特征峰,该烃的分子式可以是( )
| A. | C3H8 | B. | C4H10 | C. | C5H12 | D. | C6H14 |
1.下列固体物质属于晶体的是( )
| A. | 橡胶 | B. | 食盐 | C. | 石蜡 | D. | 玻璃 |
18.下列叙述中.不正确的是( )
| A. | 在平衡体系PCl3(g)?PCl3+Cl2(g)中加入一定量的${\;}_{\;}^{37}$Cl,达到平衡后”37Cl仅存在于五氯化鱗和氯气分子里,不可能存在于三氯化磷分子 | |
| B. | CH3C00H与H180-CH2CH3;发生酯化反应化是可逆反应,达到平衡后${\;}_{\;}^{18}$0仅存在于乙醇和乙酸乙酯分子里,不可能存在于乙酸和水分子里 | |
| C. | CH2Br2没有同分异构体的事实证明了甲烷分子是碳原子为中心的正四面体结构 | |
| D. | 在氧气中完全燃烧后生成物只有C02和H2O的有机物不一定是烃 |
5.中华文化博大精深,下列有关说法不正确的是( )
| A. | “熬胆矾铁釜,久之变化为铜”,该过程发生了置换反应 | |
| B. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 | |
| D. | 古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金 |
2.${\;}_{92}^{235}$U是制造原子弹和核发电的重要工业原料,关于铀元素的下列说法正确的是( )
| A. | ${\;}_{\;}^{235}$U的原子核外有143个电子 | B. | ${\;}_{\;}^{235}$U、${\;}_{\;}^{238}$U是同一种核素 | ||
| C. | ${\;}_{\;}^{235}$U一个原子中有92个中子 | D. | ${\;}_{\;}^{235}$U和${\;}_{\;}^{238}$U互为同位素 |
19.有机物种类繁多,有下列8种有机物,有关说法不正确的是( )
①C5H12 ②C3H6 ③CH2=CH-CH=CH2④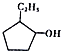 ⑤
⑤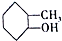 ⑥
⑥ ⑦
⑦ ⑧
⑧
①C5H12 ②C3H6 ③CH2=CH-CH=CH2④
 ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
| A. | ①和⑧是同系物 | B. | ②和③不是同系物 | ||
| C. | ④和⑤是同分异构体 | D. | ⑥和⑦是同分异构体 |
20.某化学科研小组对周围大气进行监测,发现该地区首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5微米的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx灯进行研究具有重要意义.请回答下列问题:
(1)将PM2.5样品配成待测试样,若测得该试样所含水溶性无机离子的化学组分及平均浓度如下表:
根据表中数据计算该试样的pH=4.
(2))①为减少SO2的排放,可洗涤含SO2的烟气,作为洗涤剂下列物质最好选择a(填字母).
a.氨水 b.Na2CO3 c.O2 d.NaHSO3
②浓度均为0.1mol/L(NH4)2Fe(SO4)2、NH4HSO4、(NH4)2SO3,其中c(NH4+)最大的是(NH4)2Fe(SO4)2(填化学式).
(3)①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0.汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是吸热反应,温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设计下列反应除去CO:2CO(g)═2C(s)+O2(g).已知该反应的△H>0,试判断该设想能否实现并简述理由否,因△H>0且△S<0,则在任何温度下△G>0,不可能自发进行.
(1)将PM2.5样品配成待测试样,若测得该试样所含水溶性无机离子的化学组分及平均浓度如下表:
| 离 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2))①为减少SO2的排放,可洗涤含SO2的烟气,作为洗涤剂下列物质最好选择a(填字母).
a.氨水 b.Na2CO3 c.O2 d.NaHSO3
②浓度均为0.1mol/L(NH4)2Fe(SO4)2、NH4HSO4、(NH4)2SO3,其中c(NH4+)最大的是(NH4)2Fe(SO4)2(填化学式).
(3)①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0.汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是吸热反应,温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设计下列反应除去CO:2CO(g)═2C(s)+O2(g).已知该反应的△H>0,试判断该设想能否实现并简述理由否,因△H>0且△S<0,则在任何温度下△G>0,不可能自发进行.
 )可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下:
)可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下: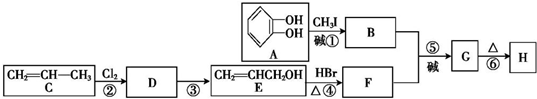
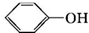 +RX$\stackrel{碱}{→}$
+RX$\stackrel{碱}{→}$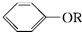 +HX(X代表卤素原子);
+HX(X代表卤素原子);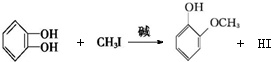 .
.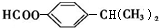 .
.